2025-07-15
文章题目:Integrated proteogenomic characterization of localized prostate cancer identifies biological insights and subtype-specific therapeutic strategies
中文标题:整合蛋白质组和基因组学分析揭示前列腺癌分子亚型及特异性治疗策略
发表期刊:Nature Communications
影响因子:15.7
发表时间:2025年
研究对象:145例中国局灶性前列腺癌患者肿瘤组织及配对非肿瘤组织
涉及组学:基因组(WES)、转录组(bulk RNA-Seq)、蛋白质组(DIA-MS)、磷酸化蛋白组、代谢组、单细胞转录组(scRNA-seq)
研究背景
前列腺癌(PCa)是全球发病率第二高的男性癌症,局灶性PCa常被归类为低或中风险,但部分患者仍会发生复发,提示现有风险分层体系存在盲点。此前的研究多聚焦于欧美人群,且多停留在基因组或转录组层面。本研究针对中国PCa人群,整合蛋白质组、基因组、转录组、代谢组和单细胞等多组学数据,构建系统性亚型分层策略,并识别出代谢相关分型及潜在治疗靶点NANS,为个体化治疗提供依据。
研究路线
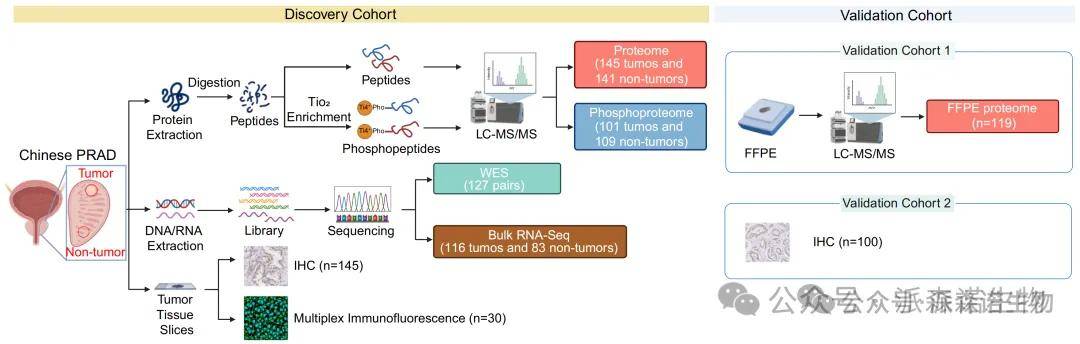
技术路线图
步骤1
多组学数据采集与构建前列腺癌图谱
研究团队收集145例PCa肿瘤与配对非肿瘤组织,开展WES、RNA-Seq、DIA-MS蛋白质组、磷酸化蛋白组及代谢组检测,并建立高质量的多组学数据平台,辅以两个独立队列进行验证。
步骤2
蛋白质组聚类构建分子亚型
基于蛋白组数据,通过非负矩阵分解(NMF)方法,将PCa患者划分为免疫型、花生四烯酸代谢型和唾液酸代谢型三种亚型,揭示其与临床特征及生化.....00000复发的相关性。
步骤3
多组学融合解析亚型分子特征
整合基因突变、SCNA、转录与磷酸化信号通路、代谢组数据等,全面描绘各亚型分子机制,锁定唾液酸代谢亚型(亚型2)为高危亚型,显著富集AR信号。
步骤4
标志物NANS识别与机制验证
通过差异蛋白分析与代谢富集定位唾液酸合成关键酶NANS,在蛋白、转录和IHC水平验证其与预后关联,并结合scRNA-seq、小鼠模型等功能实验探讨其免疫调控机制。
分析内容
1. 蛋白质组聚类建立三种功能型亚型
基于DIA-MS蛋白组数据,研究将前列腺癌分为三种功能相关亚型:免疫型、花生四烯酸代谢型和唾液酸代谢型。其中唾液酸代谢亚型(亚型2)患者PSA水平升高、GS评分较高、生化复发率最高,表现出最差的临床预后。该亚型在两个独立蛋白组和IHC验证队列中均可重复识别,并且与AR通路高度激活紧密相关,为PCa临床风险再分层提供新思路。
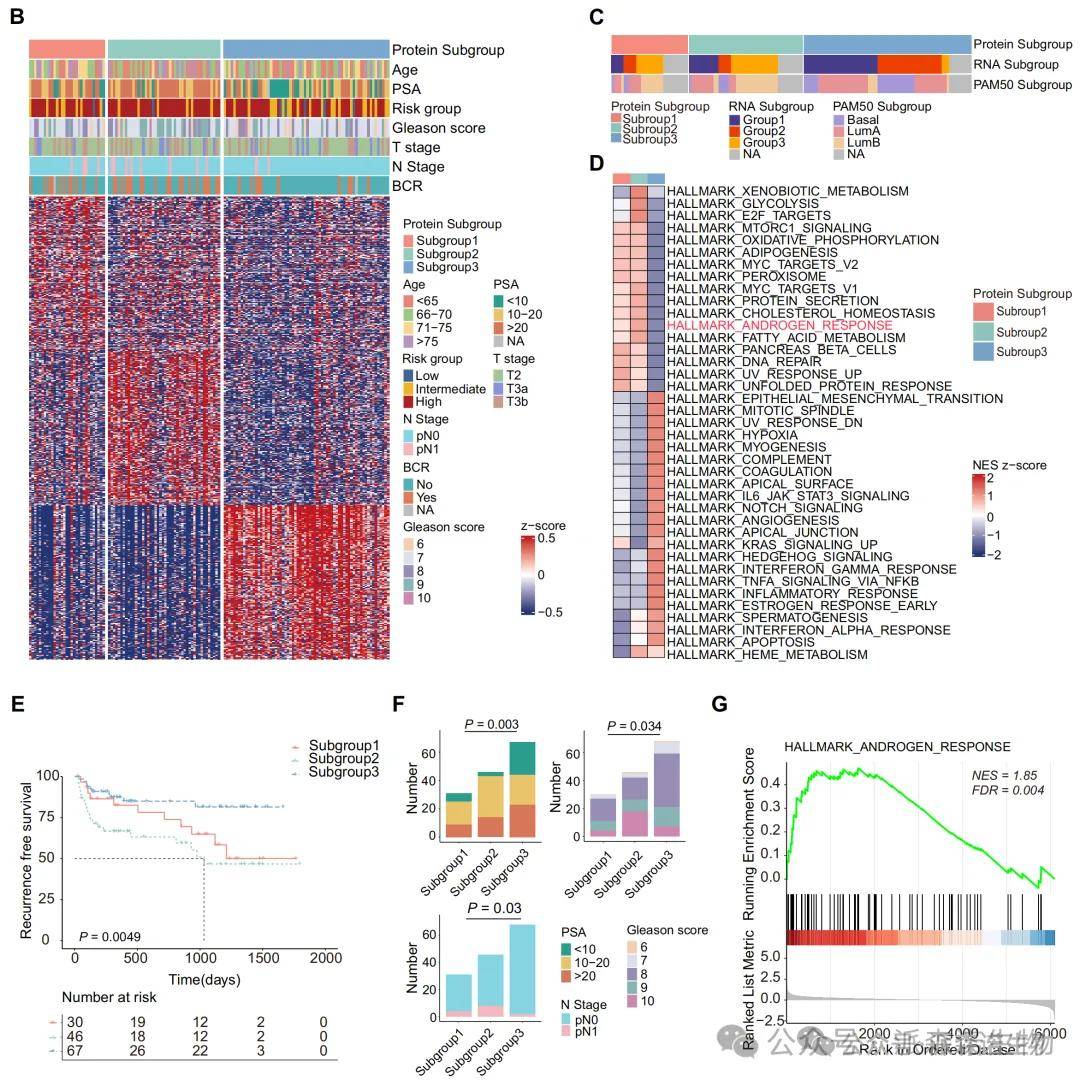
前列腺癌蛋白质组学亚型及其分子特征
2. 多组学整合揭示亚型2的遗传与信号特征
亚型2展现出更高的TMB、SCNA负荷及基因突变率,显著富集FOXA1突变、AR调控基因(GATA2、NKX3.1等)扩增和RB1缺失。转录和磷酸化数据提示AR通路及其上游激酶CAMKK2持续活跃。这些信号通路的活化机制与AR介导的去分化、增殖及免疫逃逸高度一致,凸显其治疗难度与进展风险。
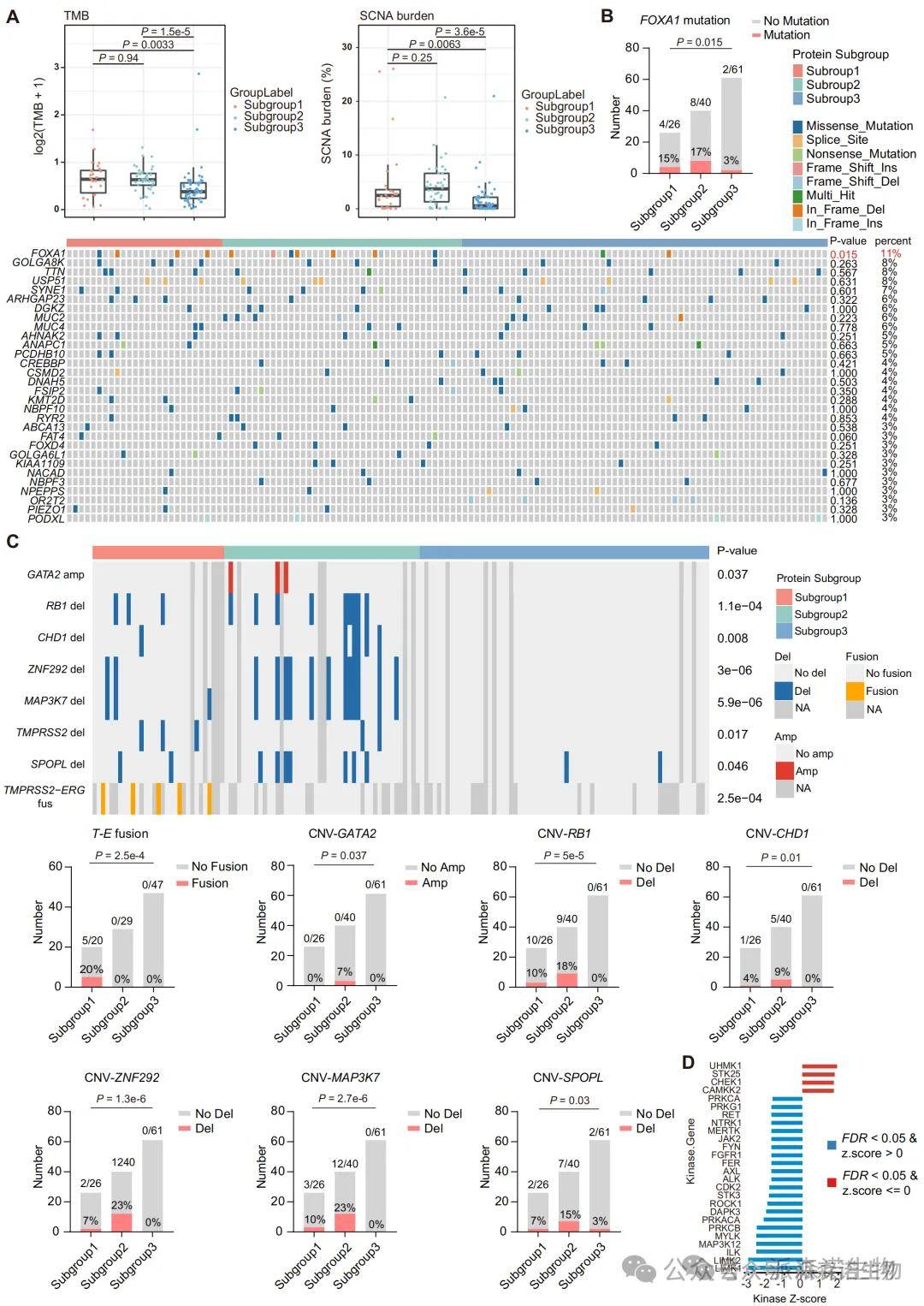
前列腺癌三个亚型的多组学特征谱
3. 唾液酸代谢显著富集并锁定关键调控因子NANS
在代谢通路富集分析中,亚型2特异性激活氨基糖及唾液酸代谢通路。NANS作为唾液酸合成关键酶,其在转录组、蛋白组及代谢组中均显著升高,并与N-乙酰神经氨酸的积累密切相关。NANS的高表达在两个独立IHC队列中均与更短BCR时间显著相关,是目前少见的可通过多组学验证的代谢标志物。
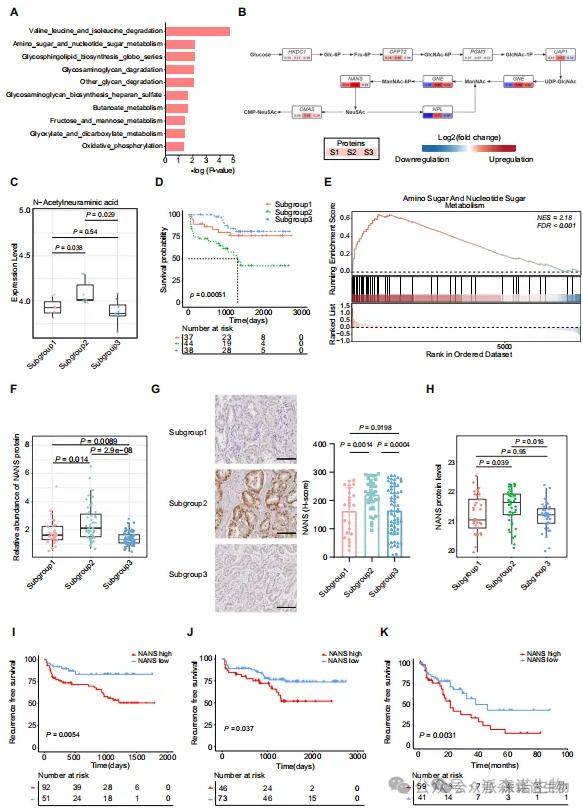
亚组2肿瘤中较高的唾液酸代谢和NANS表达与不良预后相关
4. NANS通过唾液酸化调控免疫抑制微环境
功能实验及scRNA-seq显示,NANS促进肿瘤细胞表面唾液酸化,通过与巨噬细胞Siglec受体结合招募M2型免疫抑制细胞,抑制CD8+T细胞活性。NANS敲除显著降低唾液酸水平,恢复肿瘤免疫浸润并增强免疫应答。该机制揭示了肿瘤代谢-免疫之间的直接关联,为前列腺癌的免疫治疗提供新靶点。
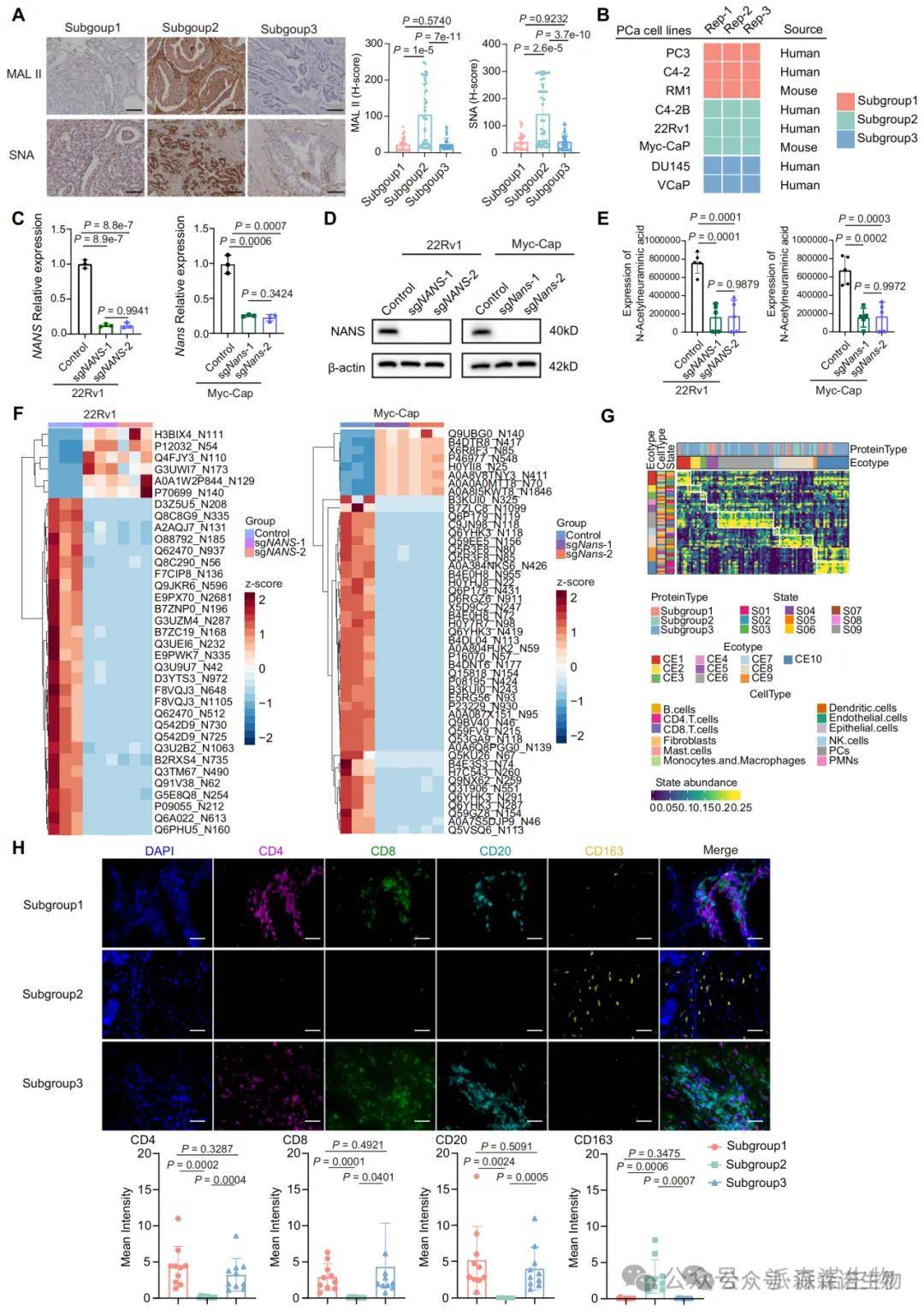
前列腺癌(PCa)免疫抑制微环境
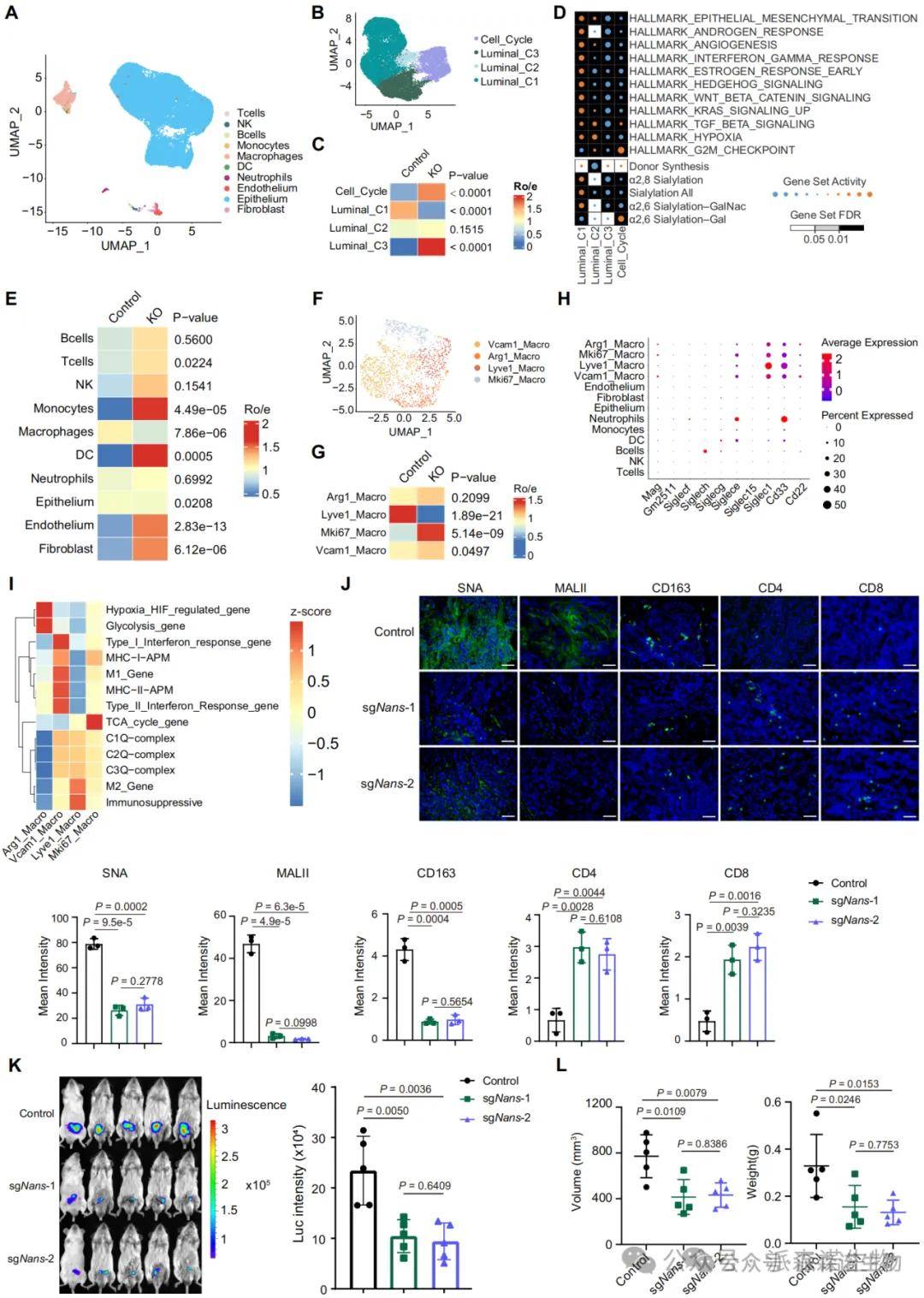
抑制NANS可逆转免疫抑制微环境
研究总结
本研究通过整合WES、RNA-Seq、蛋白组、磷酸化组、代谢组和单细胞等多组学数据,首次建立基于蛋白质表达的PCa三亚型分型系统。识别了高风险亚型“唾液酸代谢型”与AR通路激活及免疫抑制密切相关,系统锁定唾液酸合成关键酶NANS,并验证其在肿瘤免疫逃逸和预后预测中的关键作用。NANS靶向干预可逆转冷肿瘤免疫环境,延缓肿瘤进展,凸显多组学协同在肿瘤机制解析与精准治疗探索中的核心价值。


