2020-03-24

这篇2019年9月发表的揭示组蛋白标记H3K36me2招募DNMT3A并影响基因间DNA甲基化文章由来自美国洛克菲勒大学David Allis研究组、哥伦比亚大学路超研究组、加拿麦吉尔大学Jacek Majewski研究组以及清华大学李海涛教授研究组合作完成。今天我们来带大家看一下这篇文章的研究方法。
研究背景
1、催化DNA中CpG甲基化的酶,包括DNMT1和DNMT3A、DNMT3B都是哺乳动物的组织发育和体内平衡是必不可少的,它们还与人类发育障碍和癌症有关,使得DNA甲基化在细胞命运和维持中起关键作用。
2、最近的研究表明,组蛋白翻译后修饰(PTMs)参与了指定启动子上的DNMT定位和DNA甲基化模式,以及活跃转录的基因体。然而,调控基因间DNA甲基化建立和维持的机制仍然知之甚少。
3、胚系DNMT3A突变导致的塔顿布朗拉赫曼综合征(Tatton–Brown–Rahman syndrome, TBRS),是一种儿童过度生长障碍。儿童期巨脑畸形综合征(Sotos syndrome),由NSD1的单倍剂量不足引起的,其中NSD1是组蛋白甲基转移酶,催化组蛋白H3在K36位点发生二甲基化(H3K36me2)。TBRS与Sotos syndrome具有相同的临床特征。这表明这两种疾病存在机制上的关联性。
研究方法
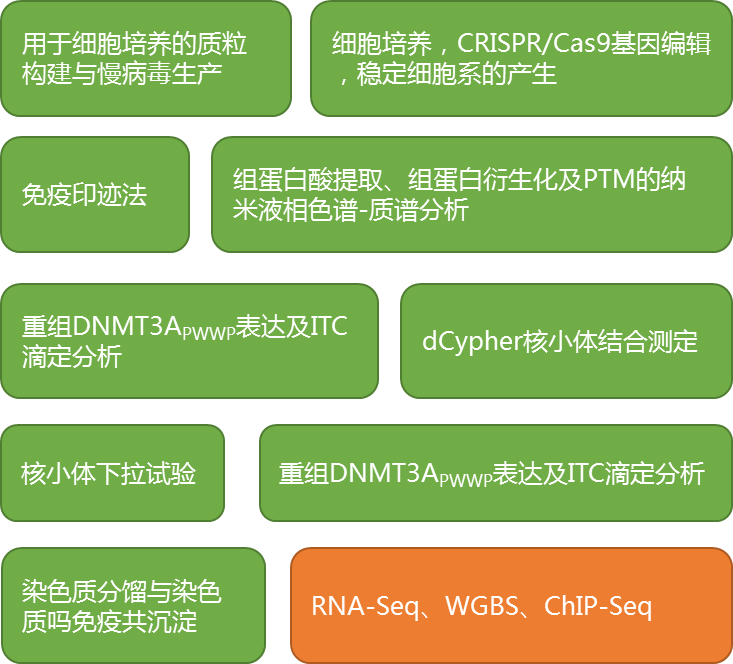
文章所用到的主要研究技术
研究结论
NSD1介导的H3K36me2是DNMT3A募集和基因间区DNA甲基化维持所必需的。全基因组分析表明,DNMT3A与H3K36me2在常染色质的非编码区同时结合并发挥作用。N在小鼠细胞中剔除基因Nsd1及其旁系同源物Nsd2导致DNMT3A重新分布到H3K36me3修饰的基因体上并且减少基因间DNA的甲基化。NSD1突变体肿瘤和Sotos患者样本也与基因间DNA低甲基化有关。因此,DNMT3A的PWWP结构域在体外显示出对H3K36me2/3的双重识别,对H3K36me2具有更高的结合亲和力,这被TBRS衍生的错义突变所消除。综上所述,我们的研究揭示了一条跨染色质调控通路,它将异常的基因间CpG甲基化与人类肿瘤和发育过度联系起来。
重要提示
由于篇幅较长,对文章研究思路与研究结果的详细介绍将在下周发出,请扫描最下方二维码持续关注我们哦!
参考文献:
Weinberg DN, Papillon-Cavanagh S, Chen H, et al. The histone mark H3K36me2 recruits DNMT3A and shapes the intergenic DNA methylation landscape. Nature. 2019;573(7773):281–286. doi:10.1038/s41586-019-1534-3.


