2020-08-10
1、TMB
肿瘤突变负荷(TumorMutationBurden,TMB)是指肿瘤细胞基因组中,所评估基因的外显子编码区每兆碱基中发生置换和插入/缺失突变(体细胞突变)的总数。
肿瘤组织中突变的基因越多,就越有可能产生更多的异常的蛋白质;这些异常的蛋白质,就越有可能被免疫系统识破,从而激活人体的抗癌免疫反应,因此对肿瘤免疫治疗的疗效就越好。

TMB如何影响肿瘤治疗效果?
在某些条件(吸烟,紫外线照射等)下,基因会发生某些治病突变,这些突变可影响转录,导致mRNA的改变,进而会产生新的蛋白质或多肽。这些新的蛋白质或多肽可被自身免疫系统识别为非自我抗原,即突变相关新抗原(mutation-associatedneoantigen),从而激活T细胞,引起免疫反应。
肿瘤细胞基因组中累积的突变数目越多,产生的突变相关新抗原(肿瘤免疫的靶点)也越多,从而可以激活更多的T细胞,产生更强大的免疫反应。因此TMB越高,肿瘤就越有可能对免疫治疗有效,理论上,做WES的TMB检测准确度非常高。
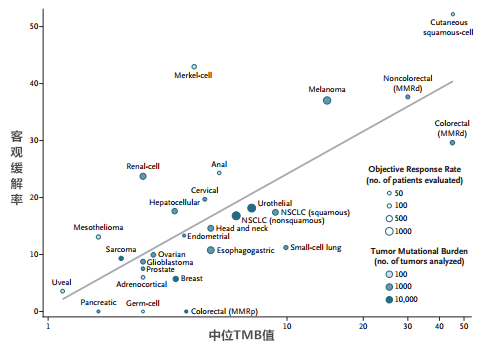
2017年底NEJM发表了一项统计数据,该数据汇总了27种肿瘤中TMB的大小与PD1抑制剂治疗的有效率的关系,结果表明不同类型的肿瘤中TMB大小不同,TMB越大,PD1/PDL1抑制剂有效率越高。

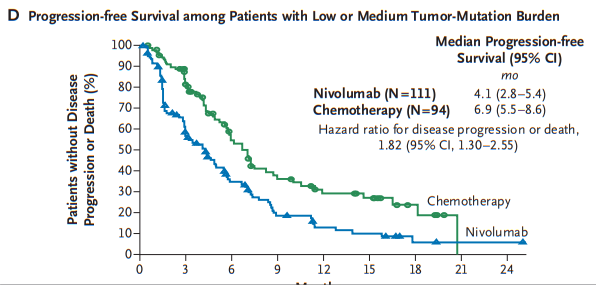
TMB与非小细胞肺癌的治疗
上图可知,非小细胞肺癌中,TMB-H的患者使用免疫检查点抑制剂的疗效由于化疗,而TMB-L的患者使用免疫检查点抑制剂的疗效低于化疗。
TMB与免疫治疗
2020年6月16日,FDA批准帕博利珠单抗(Keytruda,K药)单药治疗TMB-H(TMB≥10个突变/Mb),既往治疗后疾病进展且没有令人满意替代治疗方案的不可手术或转移性的成人和儿童实体瘤患者。这标志着TMB成为继MSI/dMMR后第二个泛实体瘤免疫治疗伴随诊断生物标志物,TMB正式成为科学领域,可帮助确定最有可能从帕博利珠单抗中受益的患者。

2、MSI/dMMR
MSI(microsatelliteinstability)是微卫星不稳定,MMR(mismatchrepair)是指基因错配修复功能。人类错配修复基因(MMR基因)经转录翻译后可表达相应的错配修复蛋白,如果任一MMR蛋白表达缺失可造成细胞的错配修复功能缺陷,则对DNA复制过程中的碱基错配丧失修复功能而造成累积,导致微卫星不稳定(MSI)的发生,约15%的结直肠癌是经由MSI途径引发的。MSI分为高度不稳定(MSI-H)、低度不稳定(MSI-L)和稳定(MS-S);MMR分为错配修复功能缺陷(dMMR)和错配修复功能完整(pMMR)。dMMR等同于微卫星高度不稳定(MSI-H),pMMR则等同于微卫星低度不稳定(MSI-L)或微卫星稳定(MSS)。

MSI/dMMR的检测意义
(1)首先是林奇综合征。如前所述,林奇综合征是由于MMR胚系突变导致个体易于发生CRC和子宫内膜癌等恶性肿瘤。对于具有上述肿瘤家族史,或者具有早发肿瘤的患者,有必要对其本人及家属进行林奇综合征的筛查,可显著降低肿瘤的发病率和死亡率。
(2)MSI可以反映预后。MSI对CRC的预后取决于分期,MSI-H是Ⅱ期CRC预后良好的指标,而转移性CRC(mCRC)虽然只有4%的为MSI-H,但这些肿瘤患者预后并不改善,特别是合并BRAFV600E突变的患者
(3)MSI可以指导后续治疗。MSI-H的II期CRC预后良好,同时对氟脲嘧啶类药物不敏感[10],因此,NCCN指南和CSCO结直肠癌诊疗指南推荐所有II期CRC均进行MSI/MMR检测,存在MSI-H的患者不推荐在治疗中加入辅助化疗。
MSI/dMMR与免疫治疗?
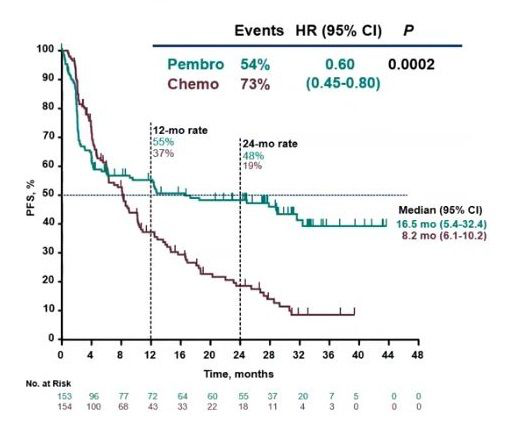
KEYNOTE-177是比较单一制剂抗PD-1疗法与标准护理化疗用于一线治疗MSI-H或dMMR结直肠癌的第一个阳性III期试验。KEYNOTE-177是一项随机、开放标签III期试验,共入组了307例MSI-H或dMMR、不可切除性或转移性CRC患者。研究中,这些患者被随机分配,接受Keytruda(每3周一次静脉输注200mg,最多35个疗程)或研究员选择的6种SOC化疗方案中的一种(mFOLFOX6;mFOLFOX6+贝伐单抗;mFOLFOX6+西妥昔单抗;FOLFIRI;FOLFIRI+贝伐单抗;FOLFIRI+西妥昔单抗)。
结果显示,与化疗相比,Keytruda单药一线治疗将疾病进展或死亡风险显著降低40%(HR=0.60;95%CI:0.45-0.80;p=0.0002)、无进展生存期延长一倍(中位PFS:16.5个月vs8.2个月)。Keytruda组2年无进展生存率为48%、化疗组为19%。Keytruda组和化疗组的总缓解率(ORR)分别为43.8%、33.1%,完全缓解率(CR)分别为11.1%和3.9%,部分缓解率(PR)分别为32.7%和29.2%。Keytruda组的中位缓解持续时间(DOR)尚未达到(范围:2.3+至41.4+)、化疗组为10.6个月(范围:2.8至37.5+)。此外,Keytruda组有83%的患者缓解持续至少2年,化疗组为35%。该研究中,59%的意向治疗人群在停止化疗组的研究治疗后接受了随后的抗PD-1/PD-L1治疗。
该研究中,Keytruda的安全性分析显示,≥3级治疗相关不良事件(TRAE)发生率低于化疗组(22%vs66%),且未观察到新的毒性反应。免疫介导的不良反应和输注反应,Keytruda治疗组发生率为31%、化疗组为13%。最常报告的免疫介导不良事件,Keytruda组为甲状腺功能减退症(12%)和结肠炎(7%),化疗组为输注反应(8%)。
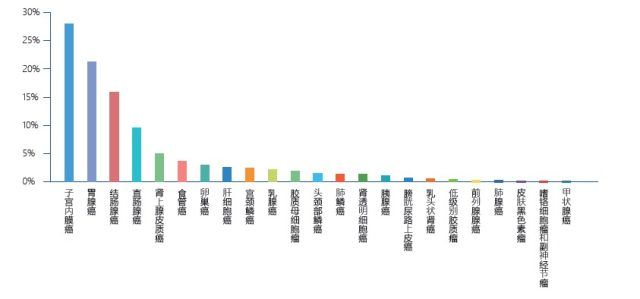
不同癌种中MSI的突变频率
FDA获批的疗法
2017年5月23日,FDA加速批准默沙东KEYTRUDA(pembrolizumab)治疗带有微卫星不稳定性高(MSI-H)的实体瘤患者,成为第一个“广谱免疫药物”。
2017年8月1日,FDA加速批准OPDIVO(nivolumab)用于治疗高度微卫星不稳定性(MSI-H)的12岁以上转移性结直肠癌患者。
2020年6月30日,FDA批准Keytruda(pembrolizumab)作为微卫星不稳定性高(MSI-H)或错配修复缺陷(dMMR)转移性结直肠癌患者的一线疗法。
派森诺医学肿瘤检测产品指导相关的免疫用药