2022-07-07
时空通讯分析导论
时间已经来到了2022年的下半页,单细胞空间的研究仍然在如火如荼地进行中,从上游的仪器制造,试剂研发,再到下游的数据分析,国内外都展开了激烈的竞争,足以说明了单细胞空间目前研究的巨大潜力和商业价值。无论是单细胞还是空间,国内都推出了国产平台,希望能在这场竞争中占据优势地位,但是10x也在不断地更新技术,保持产品的活力。对于科研者而言,单细胞级的精度与空间位置的识别仍然是生物学研究的利器,无论是发育还是疾病,时空状态的研究都不可或缺。
无论是单细胞还是空间转录组,最后分析的内容占据了很大的时间与精力,而其中细胞之间的相互作用(Cell-Cell Interaction,CCI)都是研究的重点,正常或者疾病的组织都是有机的统一体,细胞之间正确/错误的信号作用对整个组织都产生了巨大的影响,关于单细胞的通讯分析已经很透彻,本篇主要来研究时空通讯的分析内容。
时空区域通讯
细胞通讯根据不同细胞群、不同空间区域基因表达的特征,分析两者之间特异的配受体对,以此来代表细胞类型或者空间区域之间的通讯。空间转录组配受体(Spatial Transcriptomics Ligand-Receptor)分析,可以从空间转录组数据中分析配受体对的空间分布特征,揭示细胞之间在空间区域的相互交流,最终研究不同细胞类型之间的空间调控网络。其实也就是说,最开始的空间通讯研究,主要还是按照单细胞分析思路,分析clusters之间的通讯,所不同的是通讯会与空间信息关联,如下图:
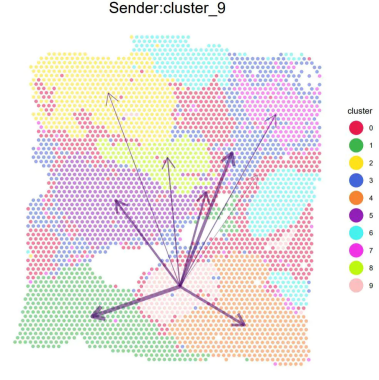
图1 时空区域通讯
这种分析思路一开始占据了主流,但是随着研究的深入,研究者们发现区域通讯存在很大的误区,首先:1、无法识别具体是哪种细胞类型起到关键的通讯作用,每个cluster都是多种细胞类型的混合体;2、空间样本的组织一般都是致密的,尤其在研究肿瘤的过程中发现了肿瘤边界的信号“开关”作用,进而推广到组织结构上的任何转换区域,都显示这种分析不够严谨,更多的是要研究组织结构的邻近区域内的通讯分析。
虽然这种方法存在严重的缺陷,但是在最开始的分析思路中起到了探路的作用,尤其在展示分析得到的配受体空间分布的时候,启发了邻域通讯的想法。
时空邻域通讯
邻域通讯的研究观点最早出现了文章Comprehensive analysis of spatial architecture in primary liver cancer[1],因为在研究中发现肿瘤和正常区域有明显的交界面,如下图:
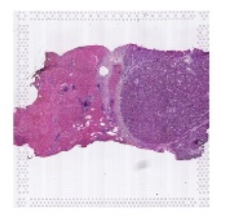
图2 肝癌样本HE染片结果
图片上明显存在一个界面,将正常区域和肿瘤区域明显地区分开,那么基于此,界面两边的通讯就至关重要,在此基础上,就有做邻近区域通讯的分析思路,如下图:
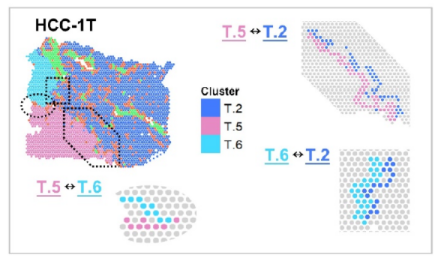
图3 时空邻域通讯
邻域通讯的关键就在于:1、找到确定位置的界面;2、分析界面两端spot的配受体对。这种方法对于组织结构的认知有一定的要求,通讯的算法方法与单细胞是一致的。
时空生态位通讯
时空邻域通讯主要还是体现在组织区域的通讯,仍然无法精确到具体什么细胞类型在起作用,目前单细胞空间联合分析已经非常普遍,细胞类型的空间分布提供了重要的结构分析,也为通讯精确到细胞类型提供了契机。因为细胞类型在空间上并不是随机分布的,特定的细胞类型会存在于特征的微环境中,也就是某些细胞类型空间上始终处于临近的位置,形成了生态位,生态位中细胞类型之间的相互通讯至关重要。
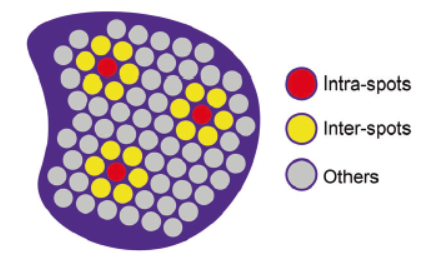
图4 细胞类型的生态位分布研究
在文章Identification of HSC/MPP expansion units in fetal liver by single-cell spatiotemporal transcriptomics[2]中就重点分析了细胞类型的生态位通讯,发现生态位形成的细胞“单元”之间的相互交流因疾病发生了明显的改变,而通过抑制这些变化为临床治疗提供了借鉴。
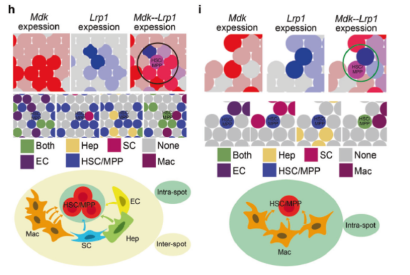
图5 时空生态位通讯
细胞在不同条件下的相互作用是一个永恒的话题,正常和疾病状态下细胞之间相互作用的变化为认知和治疗疾病提供了契机。分析细胞之间的相互作用,一方面研究细胞之间有序统一的整体是如何相互协调、维持稳态的;而通过不同条件下通讯的变化和空间分布,就可以找到疾病发生的关键点和“始作俑者”,为治疗和运用提供了借鉴。
[1]RUI WU, WENBO GUO, XINYAO QIU,et al. Comprehensive analysis of spatial architecture in primary liver cancer. SCIENCE ADVANCES, 2021. DOI: 10.1126/sciadv.abg3750. [2]Identification of HSC/MPP expansion units in fetal liver by single-cell spatiotemporal transcriptomics[J]. Cell research


