
2022-11-04

《Microbes and Infection》
影响因子:9.57
最近,复旦大学上海口腔医院和口腔医学院,在《Microbes and Infection》发表文章,建立了口服牙龈卟啉单胞菌(P.g)给药的动物模型,并评估了该模型的肝功能和病理学。分析了肠道微生物组和代谢产物。此外,评估了脾脏和肝脏中的辅助T型17细胞(Th17)/调节性T细(Treg)免疫平衡。进一步研究 P.g 在非酒精性脂肪肝病(NAFLD)中的直接作用及其潜在的分子机制。
研究背景
非酒精性脂肪肝病(NAFLD)的特征是由于非酒精性和非病毒性原因导致肝脏脂肪堆积,是西方国家最常见的慢性肝病形式,影响全球 25% 以上的人口。NAFLD常发生于中年人,尤其是超重和肥胖者。虽然预后是良性的,但非酒精性肝炎仍然是肝硬化和肝癌等不可逆疾病的严重危险因素。因此,阐明NAFLD的病理过程及其潜在机制具有重要意义。
研究表明,代谢因素引起的肝细胞内脂质异常蓄积和肝细胞死亡被认为是NAFLD的可能原因。NAFLD受多种因素影响,如一些代谢因素、药物和环境因素。此外,研究表明,由细菌菌群诱导的交替促炎或抗炎信号之间的平衡也可导致 NAFLD的进展。另外,有报道牙周病与代谢紊乱具有多向关联。牙周炎可通过口→脑轴、口→肾轴、口→心轴等一系列全身功能轴引起呼吸系统、循环系统和消化系统轻度甚至重度的病变。新出现的证据表明,牙周病会加剧肝病的进展。牙周病是一种与多种细菌相关的慢性感染性疾病,可导致牙周支持结构受损。牙龈卟啉单胞菌(P.g)是引起牙周病最重要的病原菌,它影响多种全身系统性疾病,如癌症、心血管疾病、糖尿病、类风湿性关节炎和阿尔茨海默症等。这些关联表明口→肝轴的存在,并进一步证实牙周微环境可以影响肝脏疾病。
铁死亡是一种程序性细胞死亡,其特点是二价铁或酯加氧酶催化细胞膜中高表达的不饱和脂肪酸,产生脂质过氧化作用,诱导细胞死亡。研究表明,铁死亡与许多人类疾病有关,其中铁死亡与肝脏疾病密切相关。在胆碱缺乏、补充乙硫氨酸(CDE)饮食喂养小鼠的肝脏样品中,参与脱铁途径的氧化磷脂酰乙醇胺的数量增加,表明脱铁与NAFLD有关。此外,肠道微生物通过辣椒素脂质的分泌抑制铁细胞凋亡,从而缓解肠缺血再灌注。P.g引发肠道微环境紊乱,增加了循环炎性细胞因子,并进一步影响肝脏疾病,这可能与铁死亡有关。
因此,在本研究中,为了阐明P.g在NAFLD进展中的直接作用以及潜在机制,建立了口服P.g的体内小鼠模型和与P.g共培养的肝细胞的体外模型,以分析铁死亡在关联P.g和NAFLD中的作用。
研究方法
12只6周大的雄性和12只6周大的雌性BALB/C小鼠,适应性喂养三天后,将小鼠随机分为雌雄数量相等的两组,分别为对照组和感染组(P.g),通过喂食针向每只小鼠注射200 μl脑心输液(BHI),其中感染组增加活性P.g悬浮液,实验期间,所有小鼠随意进食和饮水。在第三周和第五周,通过眶后静脉丛在身上采集大约200微升的血液。并在最后对小鼠实施安乐死,取出血液和一些器官,包括肝脏、脾脏以及上颌骨。
样品类型
小鼠粪便样品、血液、肝脏、脾脏和上颌骨组织等
研究方法
菌群多样性检测+代谢组+免疫组等
测序区域
微生物组16S rRNA基因V4-V5可变区测序
测序平台
Illumina MiSeq
分析方法
QIIME2基因云
研究结果
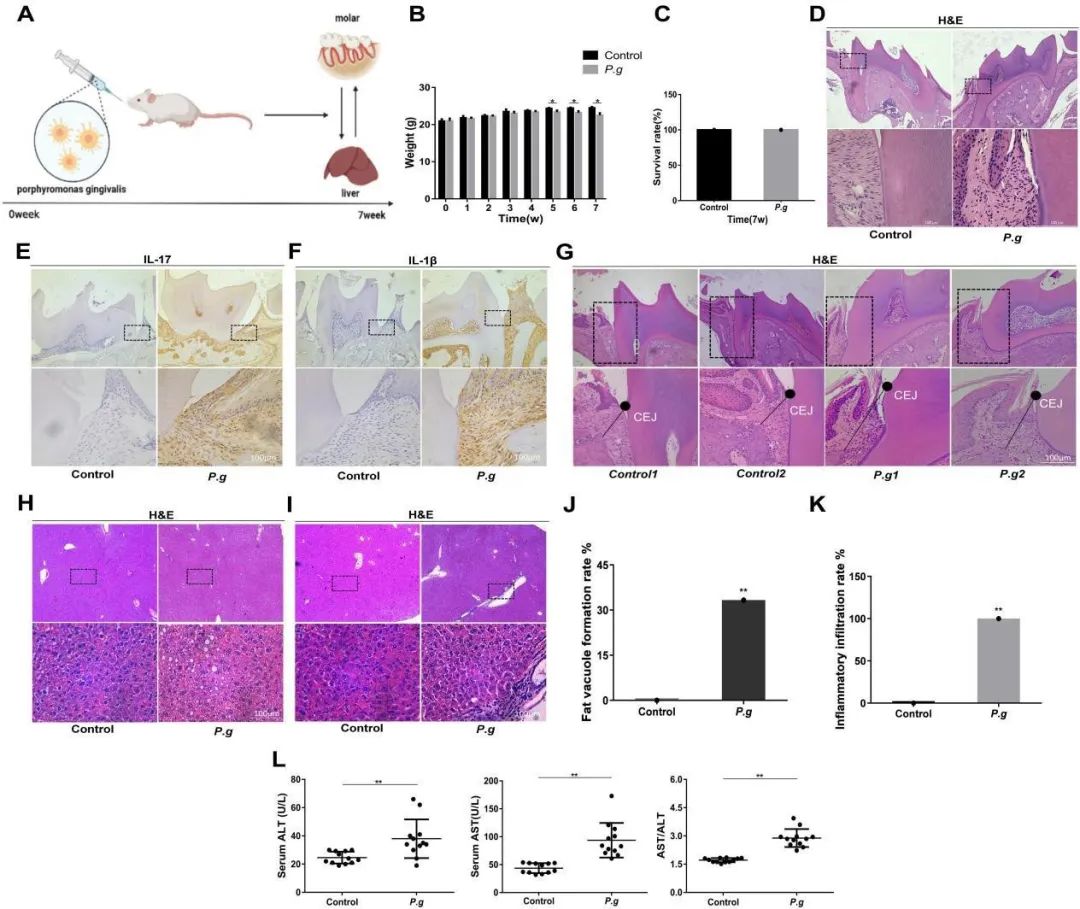
与对照组相比,P.g组在5周和7周时体重显着降低(P<0.05),而诱导期生存率差异无统计学意义(P>0.05)。此外,H&E染色结果显示P.g组牙龈有炎症细胞浸润,提示小鼠存在牙周炎。免疫组化结果显示,P.g组小鼠牙乳头处表达大量炎症因子,如IL-17和IL-1β,表明小鼠存在牙周炎症。肝切片的H&E染色结果显示P.g组中33.33%(12只中的4只)的小鼠发生肝脂肪变性(P <0.05)。所有P.g组中央静脉周围均有大量炎性细胞浸润,P.g组(100%)和对照组(P<0.05)的浸润效果有显着差异。此外,ALT和AST活性在P.g组显著增加(P<0.05)。所有这些结果表明,口服P.g给药在小鼠中可以诱导牙周炎和NAFLD。
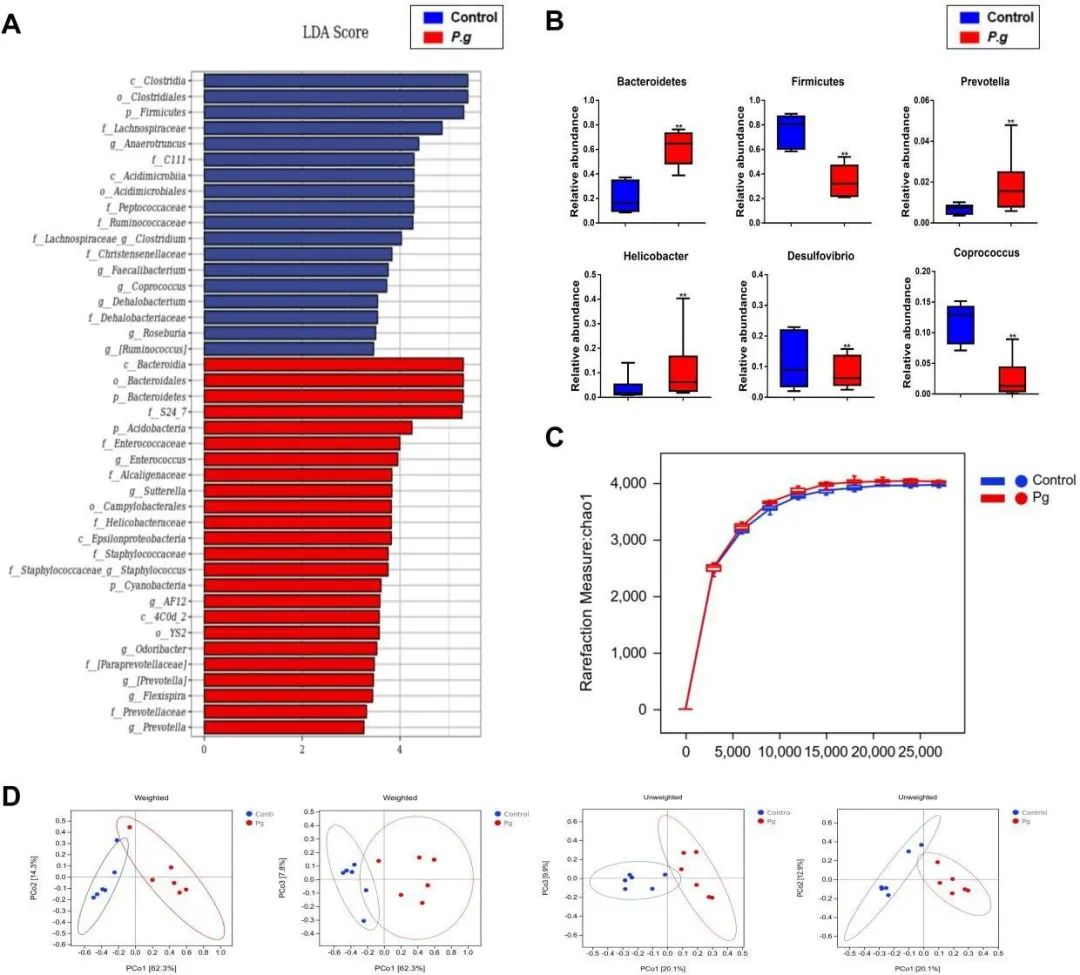
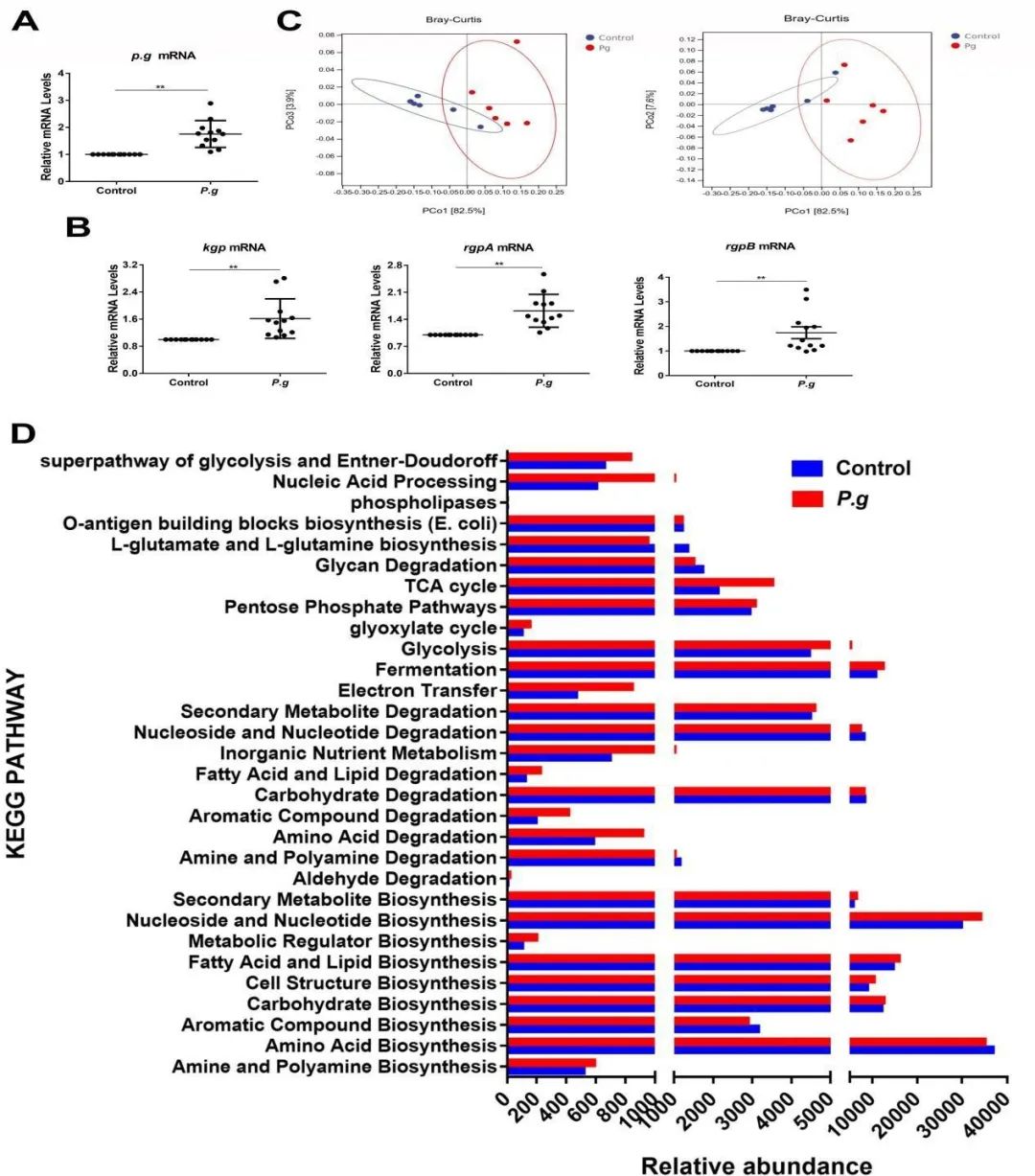
LEfSe分析表明,经P.g处理的小鼠的主要特征是存在拟杆菌科。此外,与对照小鼠相比,P.g处理的小鼠中螺杆菌和普氏菌的比例显着增加。然而,与对照小鼠相比,P.g处理的小鼠中属于厚壁菌门的粪球菌和脱硫弧菌的比例显着降低。P.g 处理的小鼠和对照小鼠之间的未加权和加权 UniFrac 距离的主坐标分析 (PCoA) 显示,P.g 给药对微生物群落的组成有明显影响。从肝组织中提取的 mRNA 的 qPCR 分析表明,肝组织中存在P.g基因片段,这表明P.g在肝脏中定植。与对照组相比,肝脏中P.g 特异性蛋白酶kgp、rgpA和rgpB的mRNA水平也显着上调。在代谢功能的潜在预测分析中,采用Bray Curtis距离算法分析P.g口服给药后的代谢功能聚类。在P.g处理的小鼠中,预测的KEGG代谢途径发生显着改变的是氨基酸生物合成、三羧酸 (TCA) 循环、脂肪酸和脂质降解等,这是与铁死亡相关的代谢途径。因此,P.g对肠道菌群和氨基酸代谢有显着影响。
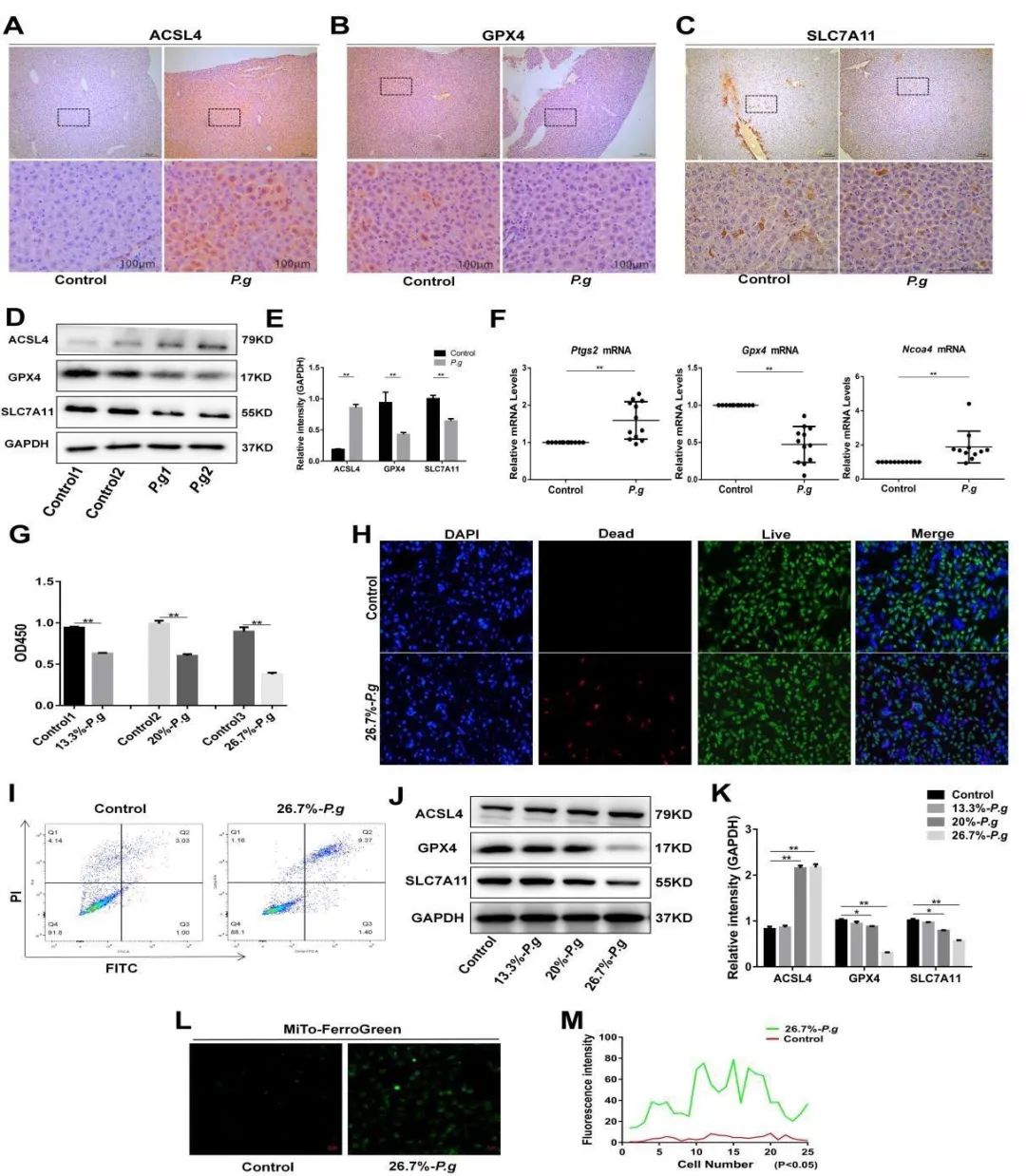
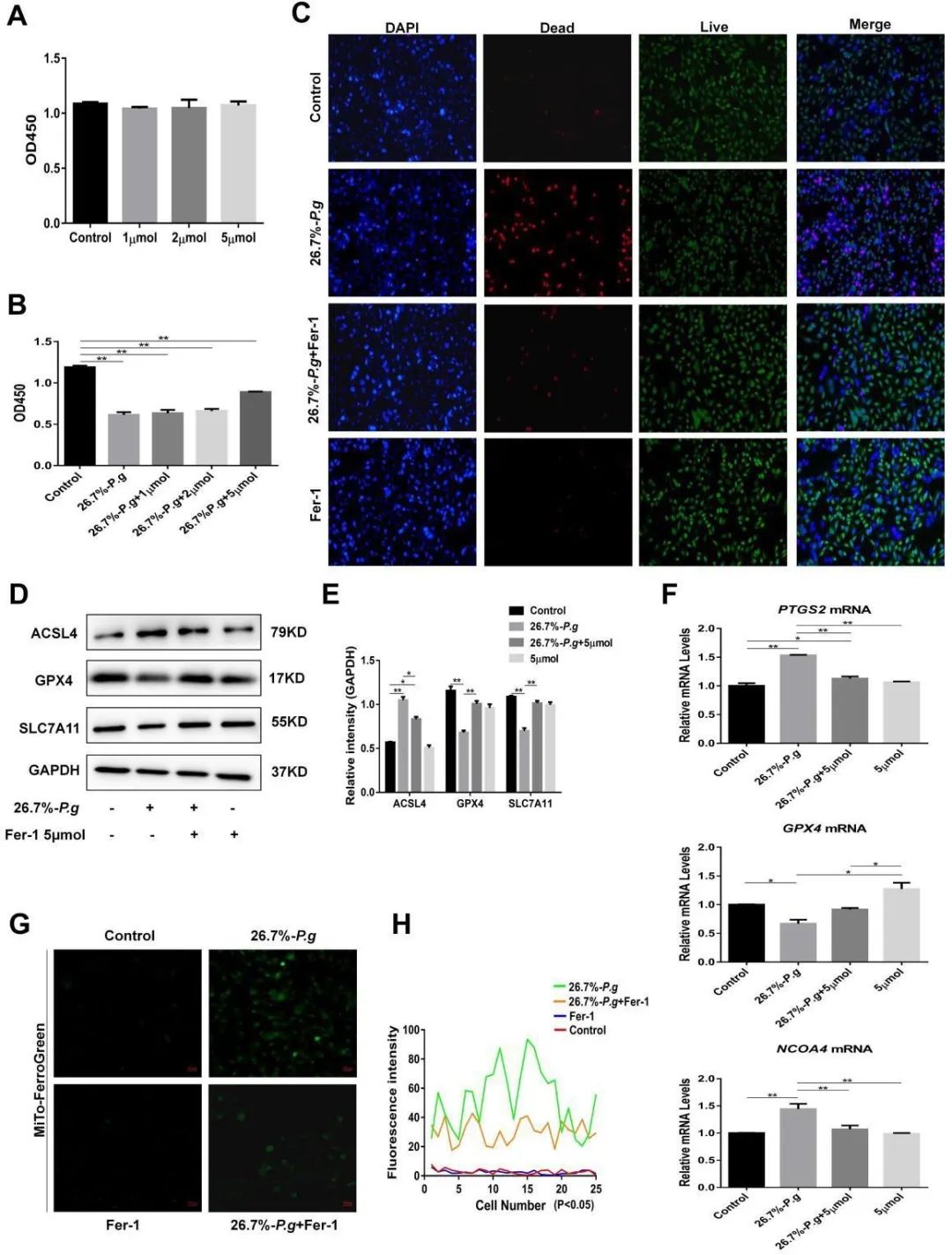
为了证明铁死亡发生在P.g诱导的小鼠肝脏病变中,我们评估了铁死亡相关标志物的水平,例如SLC7A11、GPX4和ACSL4。IHC结果显示,ACSL4 表达水平增加,而P.g中GPX4和SLC7A11表达水平降低。此外,蛋白质印迹结果显示P.g组中的ACSL4、GPX4和SLC7A11表达与IHC观察到的趋势相同。P.g组中Ptgs2和Ncoa4的mRNA水平升高,而Gpx4的mRNA水平降低。所有结果表明,P.g组的肝脏铁死亡被激活,这表明口服P.g给药后,P.g诱导了肝脏中的铁死亡。为了进一步研究P.g对体外肝脏的影响,进行了体外共培养实验。P.g的上清液在13.3%至26.7%的剂量范围内显着抑制L-02细胞的生长,而13.3%至20%的剂量与26.7%相比没有差异。接下来,活细胞和死细胞染色显示26.7%-P.g上清液显着降低了肝细胞的活力。细胞凋亡分析结果显示,与对照相比,P.g上清诱导的细胞死亡不是细胞凋亡,以上这些结果表明发生了另一种形式的细胞死亡。后续选择不同梯度的P.g上清液来验证铁死亡的发生。将不同浓度的P.g上清液与肝细胞共培养24 h,收集总蛋白。结果显示,26.7%-P.g降低了GPX4和SLCA11的表达,并增加了ACSL4的表达。因此,P.g 可在体外引起肝细胞铁死亡。
为了进一步证明P.g导致肝细胞铁死亡,在体外使用fer-1保护肝细胞免受P.g上清液的刺激。用26.7%-P.g处理肝细胞24 h后,测定细胞活力,确定铁死亡抑制剂的最佳浓度。CCK-8结果显示5 μmol fer-1对肝细胞没有毒性作用,并且它保护肝细胞免受26.7%-P.g的刺激。此外,根据活细胞和死细胞的染色显示fer-1保护肝细胞免受26.7%-P.g的影响。Western印迹结果显示ACSL4显着上调,而GPX4和SLC7A11在用P.g上清液刺激的肝细胞中显着下调。P.g组中PTGS2和NCOA4的mRNA水平升高,而GPX4的mRNA水平降低。此外,用同样的方法进行Fe2+染色,发现P.g处理组的荧光强度更强,说明P.g引起肝细胞铁死亡。然而,在fer-1处理后,P.g的荧光强度显着降低。这些结果表明P.g产物在体外可以诱导肝细胞中的铁死亡。
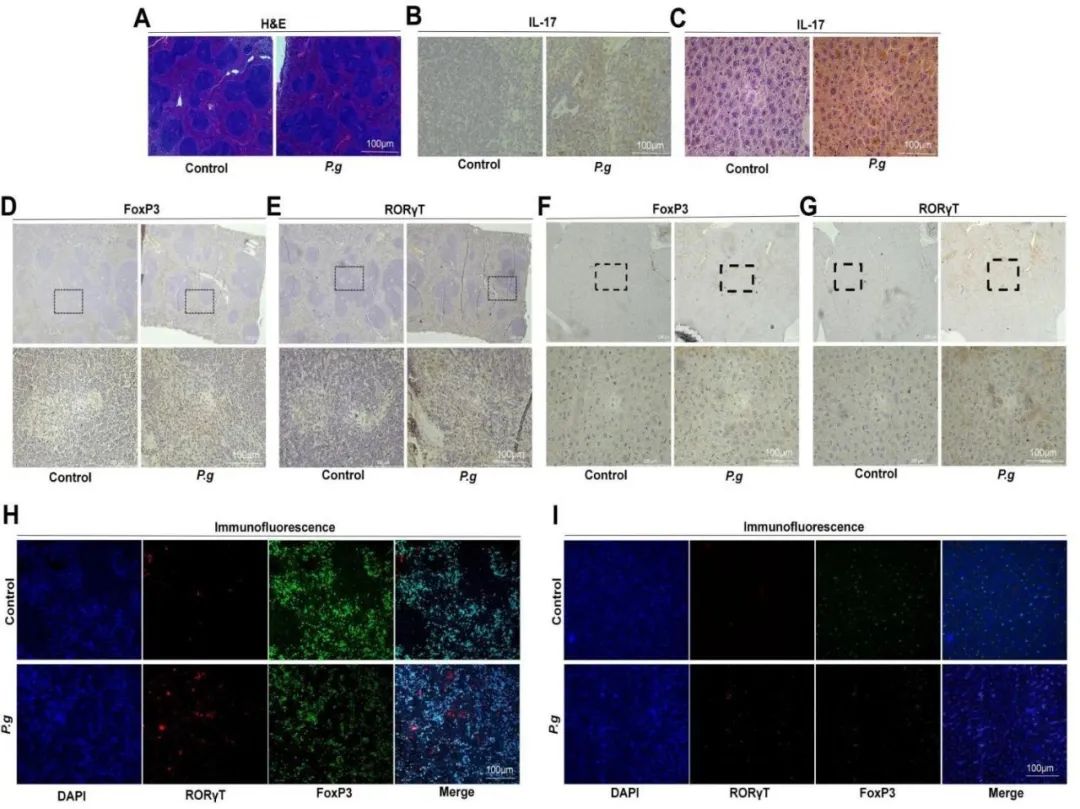
Th17细胞产生IL-17,IL-17的主要转录因子是RORγT;此外,Tregs表达转录因子是FoxP3。这些细胞分别发挥促炎和抗炎作用。脾脏H&E染色显示,与对照组相比,P.g组脾白髓已扩散至红髓,脾小梁轻度增多,提示脾脏炎症浸润。IHC结果显示,P.g组脾脏和肝脏中IL-17的表达水平高于对照组,这表明P.g触发了炎症反应。此外,P.g组脾脏中FoxP3和RORγt的表达水平高于对照组,证明Th17/Treg失衡。肝脏中FoxP3和RORγT水平的差异也显示出与脾脏相同的结果。此外,肝脏免疫荧光显示与脾脏相同的结果。与对照组相比,P.g组RORγT(红色)的表达增加,FoxP3(绿色)的表达减少。因此,P.g在体内引发了肝脏和脾脏中的Th17/Treg失衡。
总 结
在这项研究中,我们证明了口服P.g直接诱导小鼠牙周炎和NAFLD,这可能依赖于由肠道微生物代谢紊乱引起的Th17/Treg失衡引起的肝细胞铁死亡。肠道微生物代谢分析显示,与对照小鼠相比,P.g处理小鼠的氨基酸生物合成、糖和脂质代谢以及谷氨酸和谷氨酰胺合成发生了显著变化。此外,在P.g处理的小鼠的肝脏中存在P.g并激活了铁死亡,并且在与P.g产物共培养的肝细胞中也激活了铁死亡,这种效应在体外被Fer-1挽救。这些发现表明,口服P.g会影响肠道微生物群组成,使其偏向于增加一些氨基酸和炎症因子的产生,这些氨基酸和炎症因子被吸收到肝脏中,激活肝细胞铁死亡,并导致NAFLD。然而,P.g影响铁死亡的分子机制需要进一步研究。
以上研究的测序和部分数据分析工作由上海派森诺生物科技股份有限公司完成。如需进一步讨论,欢迎讨论区留言或者发邮件给我们哟(邮箱地址:metasupport@personalbio.cn)!
文章索引:
Yao C, Lan D, Li X, Wang Y, Qi S, Liu Y. Porphyromonas gingivalis is a risk factor for the development of nonalcoholic fatty liver disease via ferroptosis. Microbes Infect. 2022 Aug 17:105040.