
2022-11-25

《Nature Metabolism》 影响因子:19.865
近期,中科院微生物研究所刘宏伟/刘双江团队,在Nature集团旗下的知名期刊《Nature Metabolism》,发表重磅研究成果,可喜可贺! 本研究发现口服灵芝杂萜衍生物(GMD)能通过提高肠道粪副拟杆菌(Parabacteroides merdaede)的水平,增强肠道支链氨基酸(BCAA)分解代谢,抑制动脉斑块巨噬细胞mTORC1通路激活,发挥抗动脉粥样硬化作用,从而改善由高脂饮食(HFD)诱导的ApoE−/−(载脂蛋白E敲除)小鼠的动脉粥样硬化。该研究揭示了肠道菌群介导的改善动脉粥样硬化的一种新机制,并为调控菌群改善心血管健康提供了新的干预策略!
研究背景
心血管疾病(CVD)严重威胁人类健康,每年在全世界造成约 1700 多万人死亡。动脉粥样硬化(AS)是心血管疾病病理变化的基础,其发病机制复杂,缺乏针对性的治疗药物和手段。人体肠道微生物组学研究发现肠道菌群在心血管疾病(CVD)中发挥关键作用,多种肠道微生物来源的代谢物显示出抗或促动脉粥样硬化(AS)的作用。 在以往的研究中证明,灵芝杂萜衍生物(GMD)能够通过调节肥胖小鼠的肠道菌群,来有效改善其胰岛素抵抗、肥胖、高血糖、高血脂等代谢综合症,同时也发现在GMD治疗的肥胖、高血糖和高血脂等动物模型中,几种肠道微生物群,包括Faeciroseburia intestinalis、Parabacteroides distasonis和Bacteroides xylanisolvens显着富集。而肥胖、胰岛素抵抗、高脂血症和肠道功能障碍等是CVD的重要影响因素,所以研究人员假设GMD是否也可以借着肠道微生物群来抵抗动脉粥样硬化。 研究人员首先在高脂饮食(HFD)喂养的动脉粥样硬化ApoE−/−小鼠模型中,观察并比较GMD的治疗效果,结果发现,口服GMD可以有效改善小鼠动脉粥样硬化症状。同时证明GMD可以改变肠道菌群,使肠道共生菌粪副拟杆菌(Parabacteroides merdaede)丰度显著上升,并增强肠道支链氨基酸(BCAA)分解代谢,抑制动脉斑块巨噬细胞mTORC1通路激活,发挥抗动脉粥样硬化作用;在对公开数据及现有数据的进一步分析挖掘显示,BCAA的异常代谢和积累与胰岛素抵抗和CVD的发生发展密切相关。研究证明了靶向调控肠道菌群微生态在治疗CVD疾病中的重要潜力,为临床治疗提供了新的思路。 粪副拟杆菌Parabacteroid merdaede改善动脉粥样硬化机制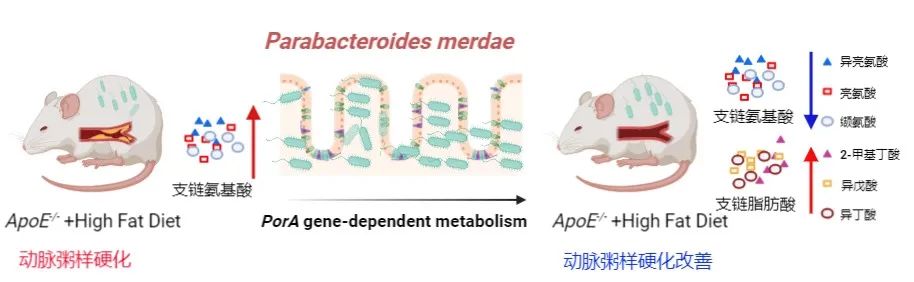
研究方法
小鼠粪便16S rRNA基因V3V4区测序+QIIME2分析流程;色谱和质谱检测分析
研究结果
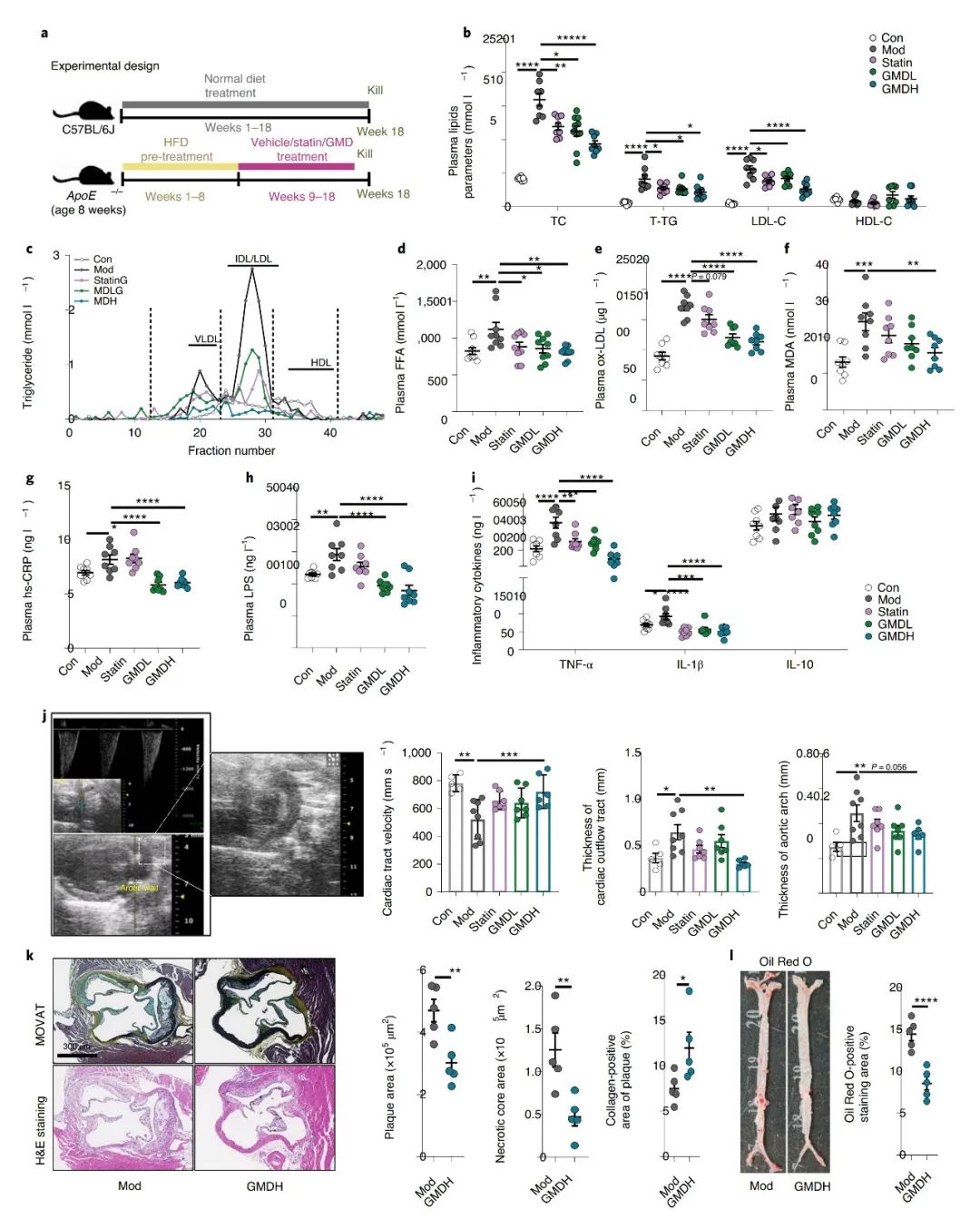
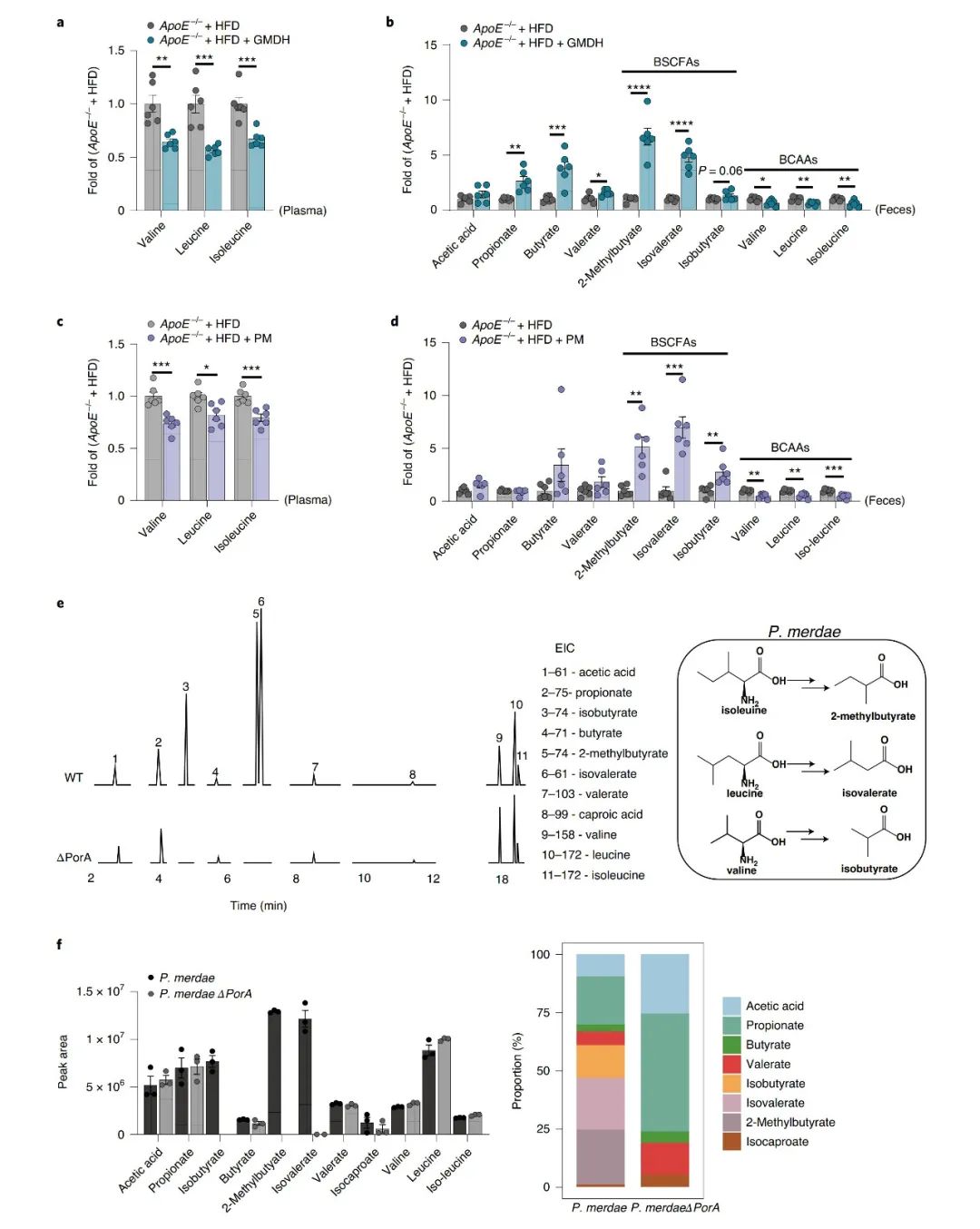
将高脂喂养(HFD)的ApoE−/−小鼠随机分组,分别服用GMD (5 mg/kg或10 mg/kg)、阿托伐他汀(10 mg/kg)或空白对照9周;同时以正常饲料喂养的C57BL/6J小鼠作为对照,结果显示,口服GMD对动脉粥样硬化的发生发展具有良好的抑制作用。 小鼠粪便样本16S rRNA基因测序分析结果显示, GMD处理组与对照组的Alpha多样性无显著差异;而Beta多样性分析显示肠道菌群的组成和丰度存在显著差异;LEfSe分析显示,模型中组中Deferribacteraceae科、Desulfovibrionaceae科、Ruminiclostridium属、Bilophila属、Anaerotruncus属、Oscillibacter属和Helicobacter bilis种显著富集,而在GMD处理组中,Tannerellaceae科、Akkermansiaceae科、Parabacteroides属、Akkermansia属、Roseburia属和Parabacteroides merdaede种, Bacteroides acidifaciens种和Bacteroides种显著富集。基于PICRUSt2软件预测获得KEGG代谢通路的相对丰度,同时通过LEfSe分析显示,GMD处理组中BCAA降解和氨基酸代谢通路显著富集。SIMPER分析量化了两组间显著变化的贡献度,结果显示,GMD处理后的粪副拟杆菌(P. merdae)丰度升高420倍,且是GMD诱导肠道菌群变化最大的贡献者。同时研究人员分析了一个来自中国的公开动脉粥样硬化队列和一个欧洲人群CVD队列的肠道宏基因组数据集,发现肠道P. merdae丰度与CVD疾病显著负相关。 为了进一步阐明P. merdae在抗动脉粥样硬化中的作用,研究人员将P. merdae活菌、热灭活的P. merdae以及PBS缓冲液分别灌胃给高脂喂养的ApoE−/−小鼠4周。结果显示,P. merda活菌处理显著改善ApoE−/−小鼠的动脉粥样硬化迹象,HFD诱导的小鼠体重、TC、T-TG和LDL-C的水平显著降低;主动脉根部病变面积、斑块区域脂肪沉积、坏死核心区域显著降低,斑块胶原蛋白水平显著上升;血浆LPS、ox-LDL、hs-CRP和肝脏脂肪变性水平降低。而热灭活的P. merda处理组并无明显改善。通过qPCR方法测定显示,ApoE−/−小鼠粪便中P. merda的相对丰度显著增加,证明其在肠道定植。P. merda处理组和模型组Alpha多样性无显著差异;Beta多样性分析显示在属和种水平上两组存在显著差异,与GMD的结果一致。P. merda的定植显著增加了HFD处理的的ApoE−/−小鼠中Akkermansia和Parabacteroides的丰度,并增强了缬氨酸、亮氨酸和异亮氨酸降解有关的代谢通路丰度。 为了确认P. merda分解代谢BCAAs的能力,对GMD或活菌P. merda处理的高脂喂养的ApoE−/−小鼠进行BCAAs和SCFAs的靶向代谢组检测。结果显示,处理组的粪便BSCFAs(包括异丁酸、异戊酸和2-甲基丁酸)显著增加,粪便和血浆中BCAAs减少,表明GMD和粪副拟杆菌对肠道中BCAA降解的影响。为了证实粪副拟杆菌对BCAAs的分解能力,对粪副拟杆菌进行体外培养,检测培养后的BSCFAs水平,结果显示,在孵育24小时后检测到异丁酸、异戊酸和2-甲基丁酸,验证了粪副拟杆菌将BCAAs转化为BSCFAs的能力。同时,为了进一步了解P. merda分解代谢BCAAs的能力,研究人员使用gutSMASH进行了泛基因组分析以识别已知和推断的基因。根据以往研究显示,在Clostridium sporogenes中,porA基因可催化BCAAs转化为BSCFAs,以该基因为依据,从P. merda基因组中鉴定出60%相似度的porA同源基因。同时,研究人员通过HUMAnN3分析了中国CVD队列肠道菌群中porA同源基因的丰度,结果显示,与健康组相比,动脉粥样硬化患者的肠道菌群中的P. merda和porA基因显著减少,对405个宏基因组数据进一步分析显示porA基因丰度与P. merda的相对丰度呈正相关。 为了验证假设,研究人员构建敲除porA的P. merda突变株(PMΔPorA),靶向代谢检测结果表明,敲除porA后,BCAAs无法转化为BSCFAs。后续为了测试porA基因依赖的BCAAs分解代谢是P. merda抗动脉粥样硬化作用机制,研究人员将PMΔPorA菌株与野生型菌株(PMWT)分别接种给HFD喂养的ApoE−/−小鼠。在porA基因的缺失不影响粪副拟杆菌定植能力情况下,与野生型菌株接种对照组相比,接种敲除porA的粪副拟杆菌的小鼠的血浆和粪便BCAAs水平显著升高,且主动脉根病变面积、斑块脂肪沉积、体重增加、血浆脂质(TC、T-TG和LDL-C)、LPS、ox-LDL、hs-CRP、TNF-α、IL-1β和IL-6均未改善。提示粪副拟杆菌在治疗肥胖相关动脉粥样硬化方面的潜力,表明porA调节的肠道BCAAs分解代谢是粪副拟杆菌抗动脉粥样硬化作用的潜在机制。 在机制方面,mTORC1信号通路的过度活化与动脉粥样硬化和胰岛素抵抗有关。根据已有研究显示,高蛋白饮食会促进动脉粥样硬化和病变,同时伴有循环亮氨酸水平的增加和斑块巨噬细胞中mTORC1信号的激活。通过免疫荧光染色PMΔPorA或PMWT处理的小鼠主动脉根,比较动脉粥样硬化斑块巨噬细胞中mTORC1通路的激活,其中下游靶核糖体蛋白S6 的磷酸化标志着mTORC1的激活。结果显示,与接种野生型粪副拟杆菌小鼠相比,接种敲除porA的粪副拟杆菌的小鼠组的斑块S6的磷酸化(pS6)显著增加,mTORC1通路激活增强。为了排除已报道的其他mTORC1诱导剂(如精氨酸或谷氨酸)的影响,靶向代谢组检测17种血浆氨基酸的水平,结果显示,在PMΔPorA和PMWT处理的小鼠之间,除BCAAs外的其他氨基酸水平均无差异。因此,BCAAs激活的mTORC1通路的调控有助于粪副拟杆菌抗动脉粥样硬化的功效。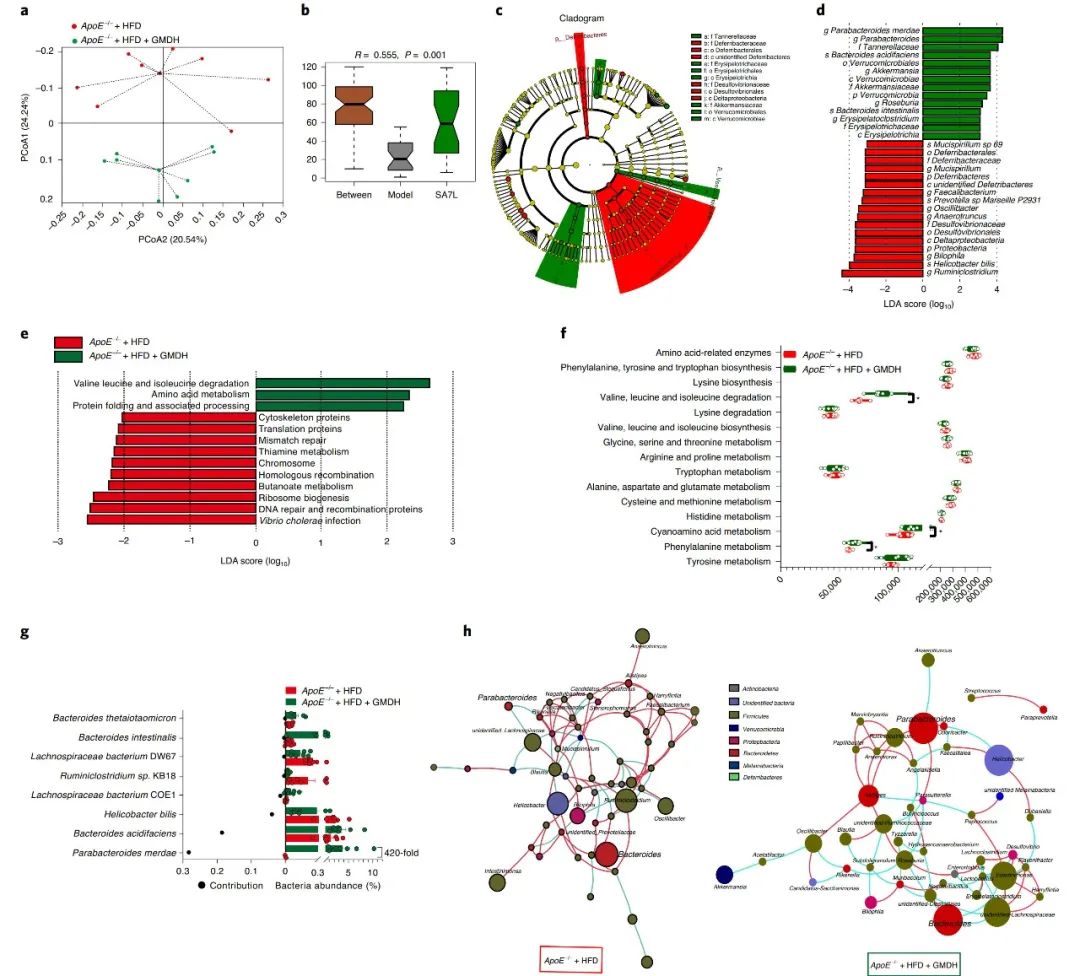
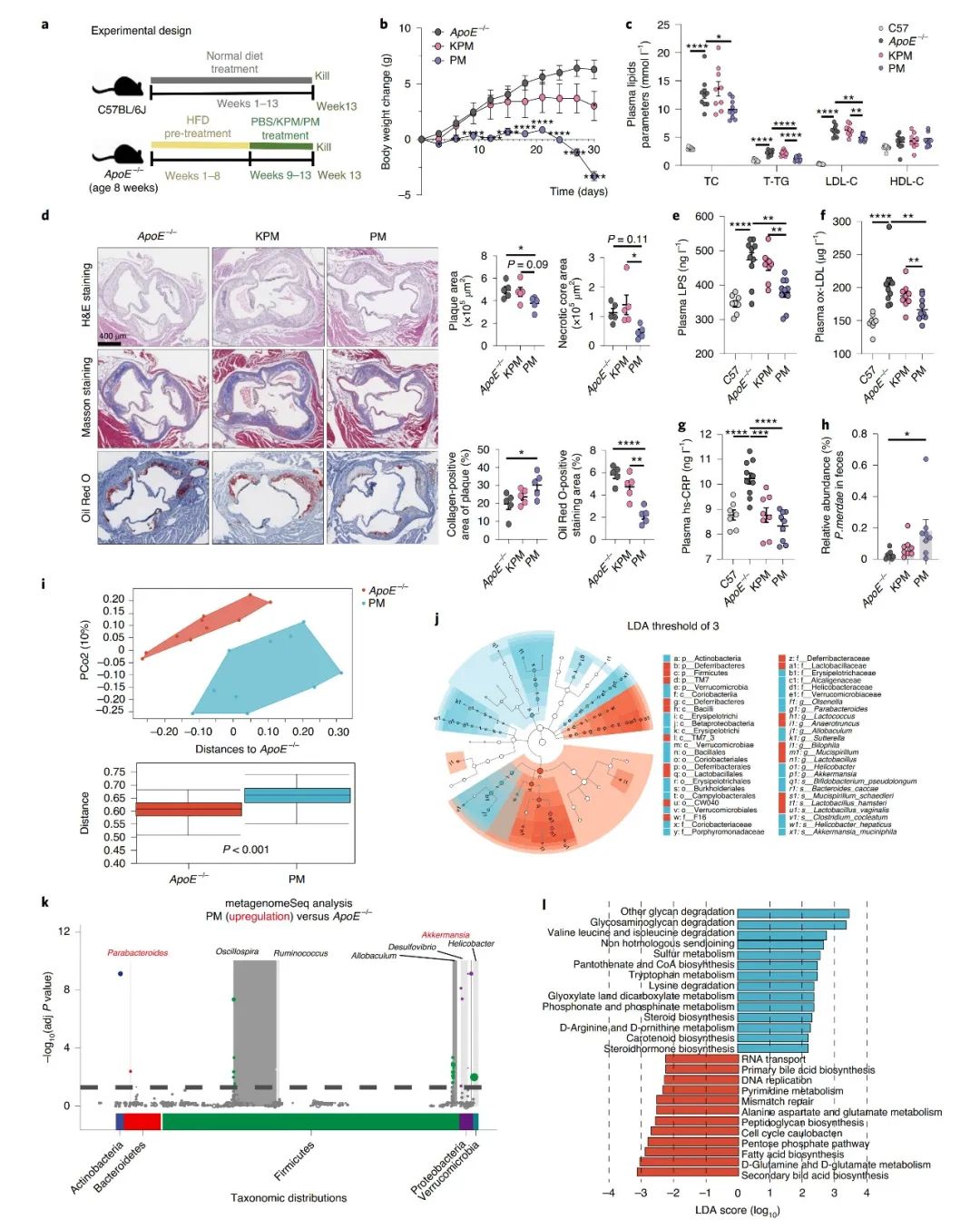

研究结论
口服灵芝杂萜衍生物(GMD)可改善高脂饮食诱导的ApoE-/-动脉粥样硬化小鼠的糖脂代谢,改善动脉粥样硬化;GMD可以改善肠道菌群,使共生菌粪副拟杆菌(Parabacteroides merdaede)丰度显著上调,并增强肠道支链氨基酸(BCAA)分解代谢,抑制动脉斑块巨噬细胞mTORC1通路激活,发挥抗动脉粥样硬化作用;P. merdaede的BCAA分解关键基因porA起介导作用,且动脉粥样硬化患者肠道菌群中缺乏P. merdaede和porA基因;GMD和P. merdaede可有效改善高脂饮食诱导的肥胖与胰岛素抵抗的动脉粥样硬化,并揭示了肠道菌群驱动的BCAAs分解代谢在维持机体心血管健康方面的重要作用。
文章索引
Qiao S, Liu C, Sun L, Wang T, Dai H, Wang K, Bao L, Li H, Wang W, Liu SJ, Liu H. Gut Parabacteroides merdae protects against cardiovascular damage by enhancing branched-chain amino acid catabolism. Nat Metab. 2022 Oct;4(10):1271-1286. doi: 10.1038/s42255-022-00649-y. Epub 2022 Oct 17. PMID: 36253620.