
2023-02-20

《Green Chemistry》
影响因子:11.034
前言 扬州大学附属医院在国际知名期刊《Green Chemistry》发表新研究成果!本研究发现一个新的HMF(1,2 5-羟甲基糠醛)高度耐受菌Enterobacter ludwigii YYP3,作为一种全细胞生物催化剂,能将HMF有效还原为2,5-双(羟甲基)呋喃(BHMF),证实了该菌株在BHMF的大规模生产中具有广阔的应用前景,而且为理解HMF还原的分子机制提供了新的见解。
01、研究背景 BHMF的脂肪酸二酯由于其高能量密度和在柴油中的优异混溶性而被认为是一类新的生物柴油添加剂。目前,化学方法仍是HMF合成BHMF的主要方法,相比之下,生物催化还原HMF,因其环境友好的反应条件、高催化效率和可选择性而被视为绿色和有前途的替代品。许多其他报道的全细胞生物催化剂中的目标酶仍然未知。更重要的是,对这些靶酶介导的HMF到BHMF转化的催化机制知之甚少。 本研究经过对Enterobacter ludwigii YYP3菌全基因组和转录组测序分析,揭示了生物催化剂耐受的分子机制,并鉴定了两种在HMF还原中起关键作用的新型短链脱氢酶/还原酶(SDR)氧化还原酶。通过结构和突变分析,揭示了HMF还原BHMF的催化机理。本研究报告的进展将为HMF向BHMF的大规模全细胞介导生物转化奠定基础。
02、研究材料与方法 1.实验材料:从化学工业土壤中分离得到的一株能够有效将HMF转化成BHMF的细菌YYP3,经过鉴定发现其为Enterobacter ludwigii。 2.测序平台:Illumina、PacBio 3.分析内容:催化效率检测、16S进化树构建、细菌完成图测序分析、转录组测序分析、蛋白结构分析等。
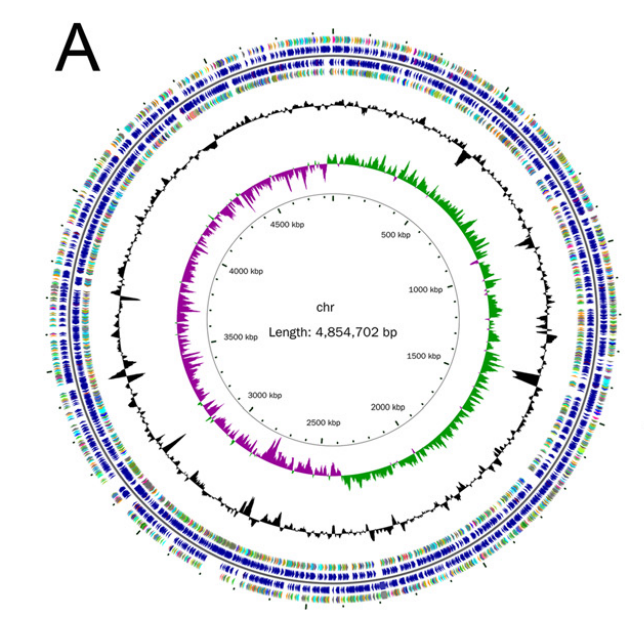
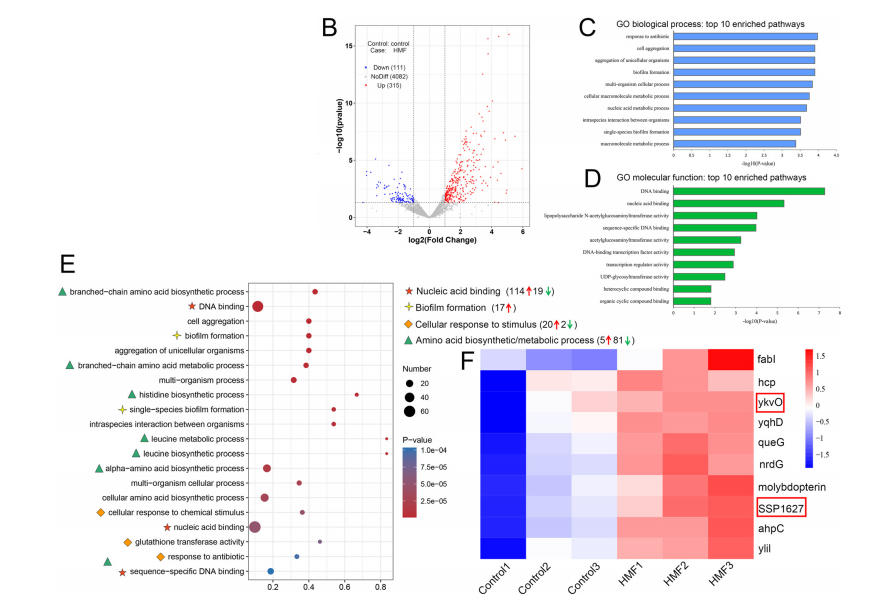
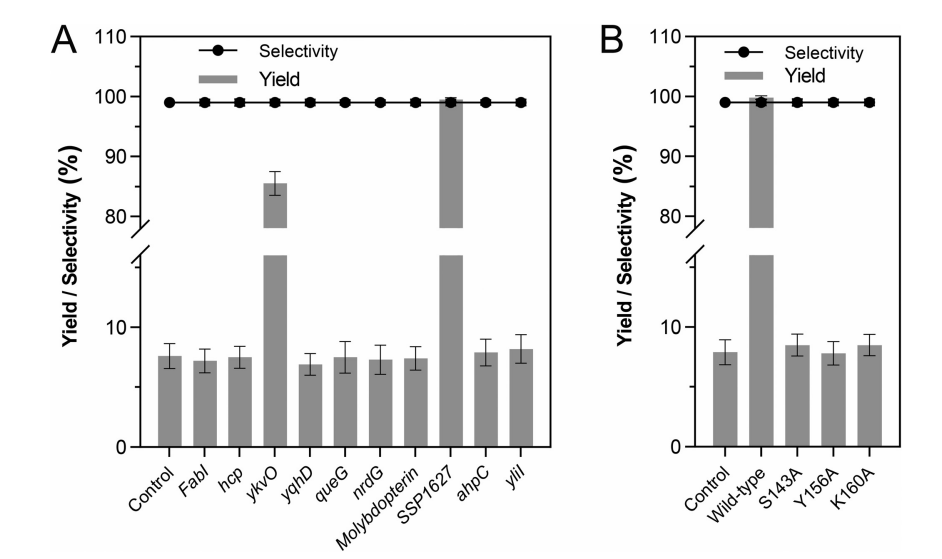
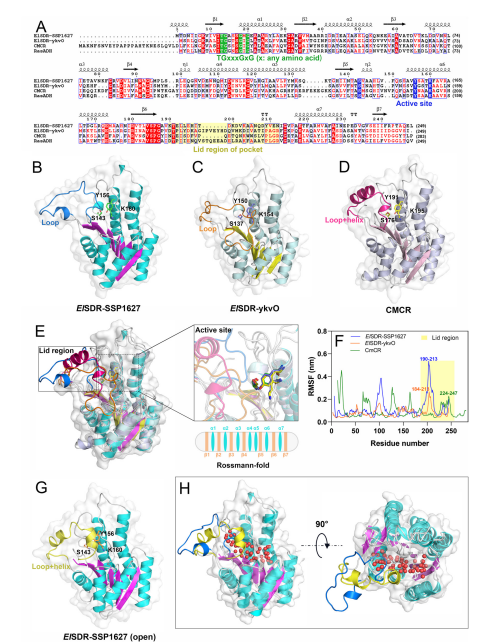
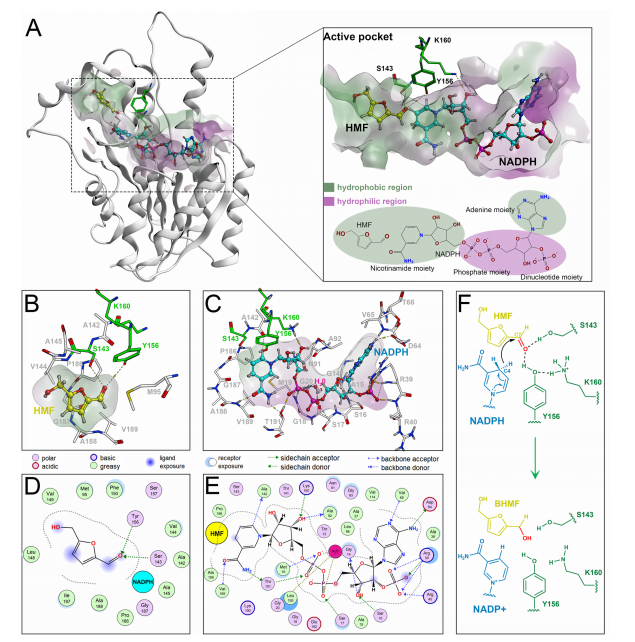
03、研究结果 E.Ludwigii YYP3对HMF生物转化的优化 从土壤样品中分离出了E.ludwigii YYP3,该细菌仅在1.5小时内转化了88.1%的HMF,对还原产物BHMF的选择性为85%,以及少量HMFCA(15%),表明对HMF具有强大的还原活性。优化后,在最佳反应条件下,E.ludwigii YYP3仅用了3小时就完全转化了100 mM HMF,BHMF产率高(>99%),选择性高(98.5%),在目前报道的全细胞生物催化剂中获得了最高的时空产率(4.2 g.L−1 h−1)。本研究中由E.ludwigii YYP3介导的生物催化过程已成为HMF绿色和清洁增值转化的化学方法的一种有前途的替代方法,因为反应可以在温和的条件下进行,具有优异的选择性和高的时空产率。 图1最佳条件下生物合成BHMF的典型过程曲线 E. ludwigii YYP3转录组测序分析 E.ludwigiiYYP3的优异性能迫使我们通过全基因组进一步研究其潜在的抗性机制,特别是负责HMF减少的靶酶。E.ludwigii YYP3的全基因组具有单个圆形染色体,其中包含4 845 702个碱基,G+C含量为54.54%,注释了4551个蛋白质编码序列、25个rRNA、84个tRNA和107个ncRNA。总的来说,在全基因组中成功注释了4502个单基因,NR、COG、KEGG、Swiss Prot、GO、TCDB、Pfam和PHI数据库分别注释了4499、4276、3031、3941、3641、1194、4008和1191个基因。通过BLAST软件对照COG数据库确定基因组功能注释,并使用GO数据库鉴定了分子功能、细胞成分和生物过程的富集分析。 图2 基因组圈图 E. ludwigii YYP3转录组测序分析 分析了暴露于或不暴露于HMF底物(100mM)的E.ludwigii YYP3的转录组数据,发现4508个基因在对照组和HMF组之间显示出不同的表达水平。在log2|fold change|>1和P值<0.05的条件下,发现315个基因上调,111个基因下调。根据GO富集分析,差异表达基因主要与生物过程和分子功能相关,包括核酸结合(114个上调基因和19个下调基因)、生物膜形成(17个上调基因)、细胞对刺激的反应(20个上调基因和2个下调基因)和氨基酸生物合成和代谢过程(5个上调基因,81个下调基因)。 图3 转录组分析结果 快速鉴定负责HMF还原的目标酶 先前已证明,具有氧化还原活性的酶最可能是这些有毒醛类还原的原因。RNA-seq发现10个编码氧化还原酶的基因在HMF实验组中高表达,推测为HMF还原的可能候选酶。异源表达结果发现,具有SDR家族氧化还原酶编码基因(ykvO和SSP1627)的重组菌株能够在50mM底物浓度下在3小时内将HMF高效转化为BHMF。有趣的是,这两种重组菌株的催化效率低于野生菌株,这可能是因为这些负责呋喃醛转化的还原酶通常是NAD(P)H依赖性的,辅因子再生也是反应中的障碍。因此,还原酶和NAD(P)H再生酶的共表达通常是必要的。 图4 BHMF转化效率 SDR家族氧化还原酶结构特征 为了进一步研究氧化还原酶对HMF还原的催化机制,分析了研究报告中的三种酶(CmCR、MgAAD1669、AspRedAm)以及两种SDR(ElSDR-ykvO和ElSDR-SSP1627)的氨基酸序列和结构。它们之间最大的构象差异是活动袋顶部的盖区。在ElSDR-ykvO和ElSDR-SSP1627中,有一个无序的长环屏蔽活性位点,而在CmCR中有一个短环和α-螺旋保持活性位点相对开放。分子动力学模拟表明,ElSDR-ykvO和ElSDR-SSP1627盖区的RMSF值明显高于CmCR,这意味着更大的灵活性。因此,综合上述结果,两种SDR和CmCR盖区的结构和柔性差异可能会对其从HMF到BHMF的还原活性产生很大影响。 图5 ElSDR-SSP1627、ElSDR-ykvO和CmCR与SDR家族醇脱氢酶RasADH的序列比对及蛋白结构 SDR家族氧化还原酶还原HMF的催化机理 袋状结构特征分析表明:HMF和NADPH的烟酰胺和腺嘌呤部分占据了空腔的疏水区域,而NADPH的二核苷酸和磷酸部分位于空腔的亲水区域内。分子对接结果表明,HMF的羰基氧与S143和Y156的羟基之间形成了两对氢键相互作用。共底物NADPH通过与许多周围氨基酸残基的氢键相互作用(16个氢键)而大大稳定。结合以上结果,我们推测ElSDR-SSP1627介导的HMF还原的催化机制也基于HMF还原中的活性位点Ser、Tyr和Lys。由于ElSDR-ykvO、ElSDR-SSP1627和CmCR具有相似的结构和催化中心,我们认为与HMF还原相关的SDR可能共享这种催化机制。 图6 ElSDR-SSP1627与HMF(黄色)和NADPH的分子对接结果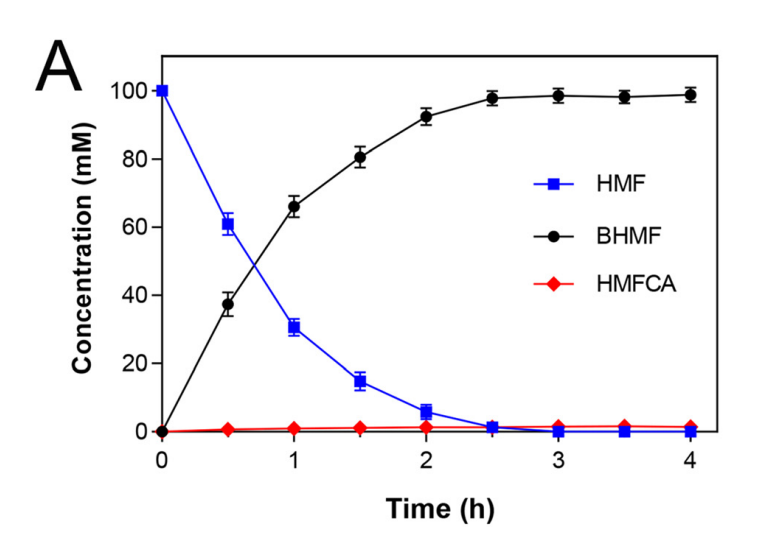
04、研究结论 在我们的研究中,发现了一种新型的全细胞生物催化剂E.ludwigii YYP3,在从HMF合成BHMF中表现出优异的催化效率和循环稳定性。经过细菌全基因组和转录组测序,揭示了HMF耐受的分子机制。同时,两种新的SDR家族氧化还原酶,ElSDR-ykvO和ElSDR-SSP1627,被鉴定用于将HMF转化为毒性较小的BHMF,其催化机制被认为是基于活性位点Ser、Tyr和Lys。了解这些机制将有助于我们通过代谢工程和合成生物学进一步提高全细胞生物催化剂的催化性能。
本研究的细菌完成图和转录组测序及分析由上海派森诺生物科技股份有限公司完成。如需进一步讨论,欢迎发邮件或者致电我们哟(邮箱地址:microsupport@personalbio.cn,联系电话:021-80118168-8617)!
文章索引:Pan X., Wang X., Wu S.H., et al. (2022).Insights into the molecular mechanism of a new effiffifficient whole-cell biocatalyst Enterobacter ludwigii YYP3 in 5-hydroxymethylfurfural reduction.Green Chemistry. DOI: 10.1039/d2gc01967arsc.li/greenchem.