
2023-06-26

《Microbiome》
影响因子:16.837
近日,西北农林科技大学在微生物领域的《Microbiome》发表新研究成果!本研究发现益生菌能增强宿主对病原体感染的抵抗力主要取决于一种厌氧的索氏鲸杆菌产生的维生素B12的功能。此外,维生素B12作为一种肠道微生物调节剂,表现出加强肠道微生物群和肠道屏障紧密连接和相互作用的能力,从而提高宿主对病原体感染的抗性。
研究背景
现在抗生素是治疗病原体感染的常用方法,但长期使用可能导致细菌耐药性以及其他健康风险。益生菌可通过改善屏障功能、免疫调节、代谢功能和抑制潜在病原体四个机制发挥作用。此外,益生菌的存在也可以诱重塑肠道原生微生物群落。本研究以枯草芽孢杆菌和斑马鱼分别作为益生菌和动物模型,描述了益生菌调节斑马鱼肠道共生菌对宿主抵抗病原体感染的作用。
研究材料与方法
1.实验材料 B. velezensis strain1704-Y 2.测序平台 Illumina + PacBio 3.分析内容 细菌基因组完成图测序、16S多样性测序、PLS-PM分析等。
研究结果
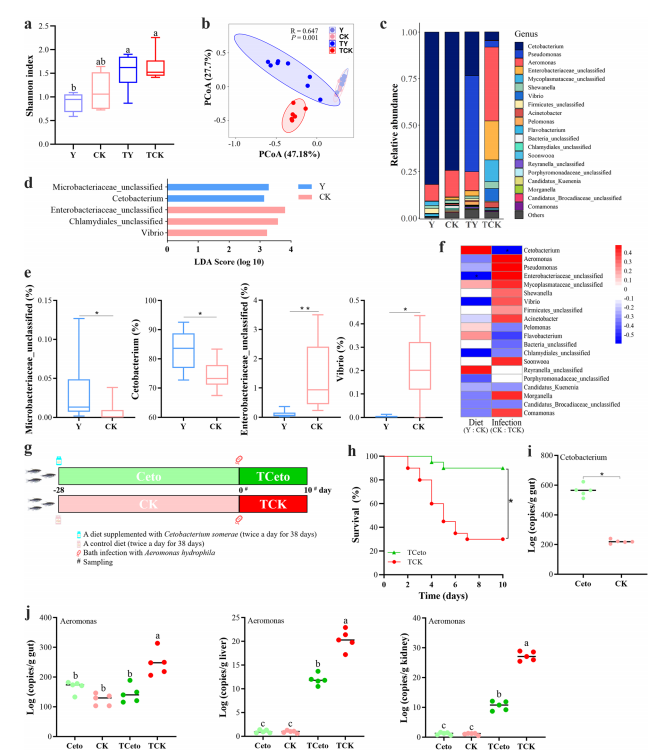
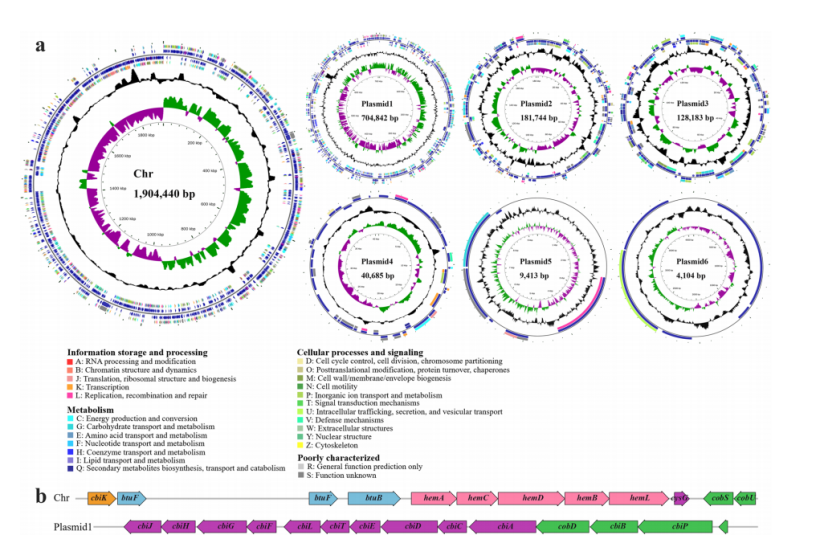
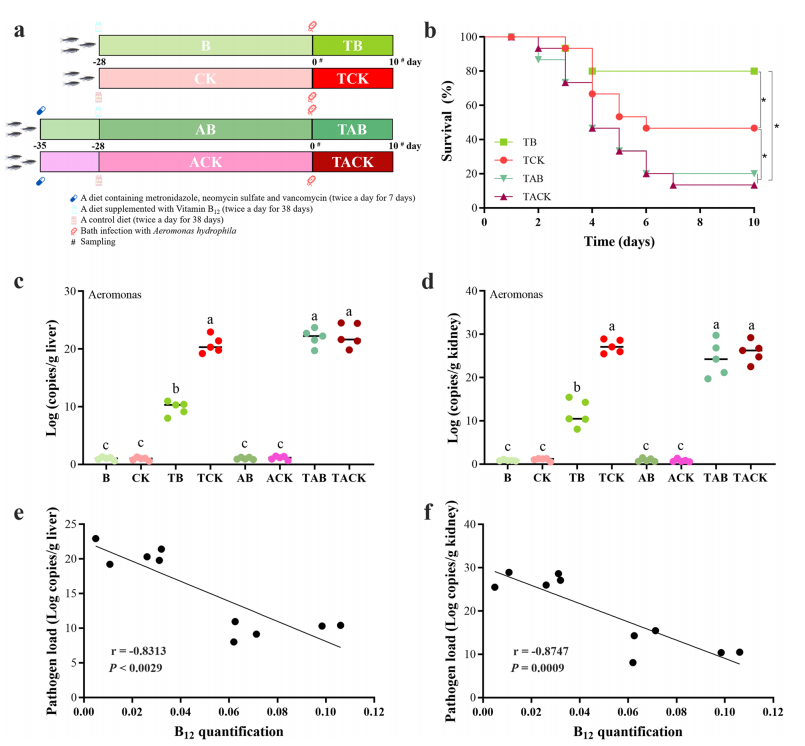
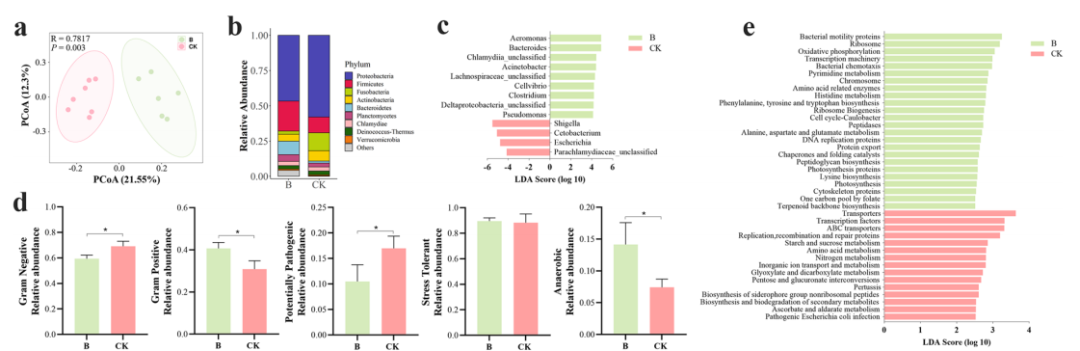
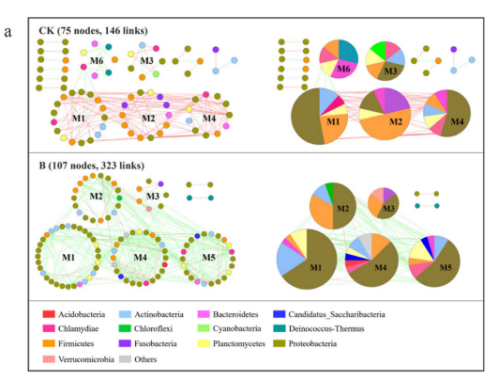
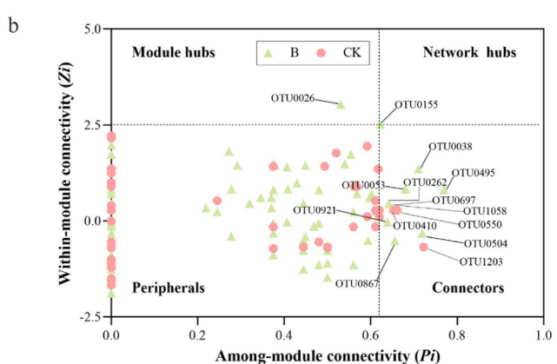
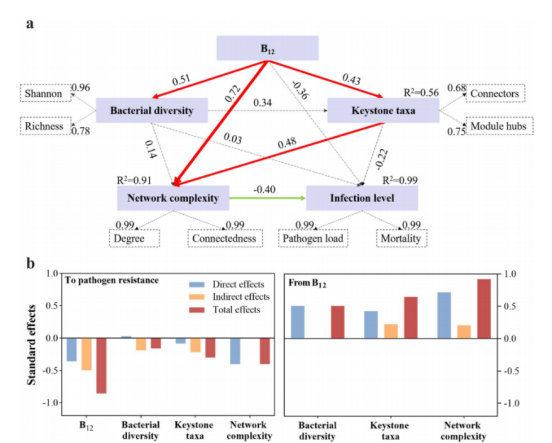
1. 益生菌对嗜水气单胞菌感染的保护作用取决于肠道微生物群 从斑马鱼肠道中分离出一株细菌1704-Y,经形态学观察和gyrB基因系统发育树鉴定为贝莱斯芽孢杆菌,并通过溶血和抗生素敏感性试验证明其对斑马鱼具有潜在的安全使用价值。同时,根据之前的研究,发现与抗生素混合的饲料消除了口服补充BV1704-Y的保护作用,从而表明肠道微生物群在保护斑马鱼免受嗜水气单胞菌感染中发挥了关键作用。 图1 1704-Y对斑马鱼预防致病性感染的影响 2. 索氏鲸杆菌对抵抗对嗜水气单胞菌感染起到重要作用 为了确定肠道菌群如何影响BV1704-Y诱导的保护作用,首先采用16S rRNA多样性测序方法比较研究口服给药前后肠道菌群组成。α-多样性结果表明,有无BV1704-Y的饲料间的细菌丰富度和多样性没有明显差异。但主坐标分析(PCoA)显示,BV1704- Y喂养的斑马鱼与对照组的细菌群落明显不同。此外,肠道微生物群在门和属水平上的组成也显示了不同类群间肠道微生物群的差异,其中鲸杆菌是核心微生物中相对丰度最高的属。 索氏鲸杆菌CS2105-BJ为杆状细胞、中央肿胀、革兰氏染色阴性和微耐气性。在感染实验中,CS2105-BJ组喂食的斑马鱼在感染后的存活率明显高于对照组,且饲料中含CS2105-BJ显著增加了斑马鱼肠道的类细菌负荷,并显著降低了感染后10天鱼肠道、肝脏和肾脏的嗜水气单胞菌。总的来说,这些数据表明斑马鱼肠道中的索氏鲸杆菌对保护斑马鱼免受细菌感染做出了重大贡献。 图2 索氏鲸杆菌对抵抗嗜水气单胞菌感染起到重要作用 3. 索氏鲸杆菌的全基因组注释分析 索氏鲸杆菌CS2105-BJ包含一条染色体(1,904,440bp)和六个质粒(质粒1:704,842bp;质粒2:181,744bp;质粒3:128,183bp;质粒4:40,685bp;质粒5:9,413 bp;质粒6:4,104bp)平均GC含量为29.15%。共预测了2,732个蛋白编码基因,其中2,371个(86.7%)基因注释为功能基因,361个(13.3%)基因注释为假设基因。在索氏鲸杆菌CS2105-BJ基因组中未发现毒力因子。此外,COG注释结果显示,CS2105-BJ基因组具有一组完整的维生素B12从头合成所需的基因,也称为氰钴胺素。 众所周知,B12可以为人类和动物的健康提供多种有益的功能,如保护肠道免受胃溃疡的侵袭,调节肠道微生物生态,以及刺激免疫反应。此外,最近的一些数据表明,B12能够有助于宿主防御致病性感染。因此,推测提高斑马鱼对嗜水气单胞菌的抵抗力与CS2105-BJ基因组上的B12生物合成有关。B12的产量随着体外细菌的增殖而增加,此外口服补充索氏鲸杆CS2105-BJ显著提高了斑马鱼肠道中的B12水平。同时发现肠道微生物产生的维生素B12在保护宿主免受嗜水气单胞菌感染中起着关键作用。 图3 基因组分析 4.B12对嗜水气单胞菌感染的保护作用依赖于肠道微生物群 饲料中添加B12显著提高了斑马鱼感染后的存活率,且与TCK组的对照组相比,TB组的斑马鱼的肝脏和肾脏中的嗜水气单胞菌负荷也降低了。此外,观察到肝脏和肾脏中B12水平与嗜水气单胞菌负荷之间的强负相关关系。这些结果表明,B12在预防嗜水气单胞菌感染方面具有保护作用。先前对斑马鱼的研究表明,抗生素的使用可以破坏和清除肠道微生物。在喂食试验之前,用含有混合抗生素的饲料喂养斑马鱼,以耗尽共生微生物。在斑马鱼感染嗜水气单胞菌后,没有观察到肝脏和肾脏中气单胞菌负荷的下降,这伴随着保护作用的消除。此外,还发现B12对斑马鱼的保护作用是浓度依赖性的,推测有一小部分高外源性B12未被吸收,到达远端肠道,在那里它们可以与微生物群相互作用。 图4 肠道微生物群是B12保护斑马鱼减少嗜水气单胞菌感染的基础 5.维生素B12诱导肠道微生物组结构和功能的改变 对照组和B12补充组两组之间存在明显的分离性,这表明饲料中添加B12显著改变了肠道微生物群落结构,且喂食维生素B12的斑马鱼在感染嗜水气单胞杆菌后肠道微生物群落组成更稳定,说明膳食中添加B12对肠道健康有很大的贡献。进一步评估两组间细菌组成变化,发现B12补充组中与肠道微生物群失调相关的志贺氏菌和大肠杆菌减少,而许多潜在的有益微生物增加。厌氧菌是维持肠道内稳态的关键调控因子。B12处理后,厌氧菌的相对丰度显著增加,说明B12可能促进了肠道中厌氧微生物的富集。添加B12显著提高了肠道微生物群的多样性和群落结构,也影响了肠道的氧化还原状态,改善了肠道菌群之间的相互作用。 图5 维生素B12诱导肠道微生物群结构和功能的改变 6. B12增强了肠道生态网络的复杂性和稳定性 通过CK和B网络中的大模块分析以及B12摄入后肠道微生物相互作用的潜在变化,发现B的肠道微生物生态网络比CK的更稳定。此外,补充B12后,模块中OTUs的组成发生了显著改变。在CK网络中,变形菌门和厚壁菌门占主导地位,而在B网络中,只有变形菌门占主导地位。在本研究中,在B网络中只检测到一个网络枢纽和一个模块枢纽。同时,与CK网络相比,B网络有更多的连接器,说明B12的补充显著增强了肠道菌群之间的相互作用关系。有趣的是,检测到的网络枢纽(OTU0155)和模块枢纽(OTU0026)以及大多数连接器都是罕见的类群,表明较少的细菌在微生物生态网络中发挥调节作用。 图6 维生素B12注入肠道生态网络 通过构建PLS-PM模型去量化关键类群和网络复杂性对宿主的病原体抗性的影响,结果表明,添加B12主要通过注入肠道中潜在的关键物种,提高肠道微生物生态网络的复杂性,来提高宿主对病原体的抗性。 图7 PLS-PM分析结果及B12增强了斑马鱼肠道内的紧密连接结果 7. B12维持了病原体感染后肠道紧密连接蛋白的正常表达 肠道屏障的通透性是病原体形成肠道感染结果的基础,因此,通过Western blot(WB)检测了肠道中主要紧密连接蛋白(Claudin15、Occludin和Zo-1)的表达。结果显示,添加B12显著上调了Claudin15、Occludin和Zo-1。相比之下,ACK和AB之间的Claudin15、Occludin和Zo-1的表达没有差异。这表明,B12注入的肠道微生物群网络维持了病原体感染的斑马鱼中肠道紧密连接蛋白的正常表达。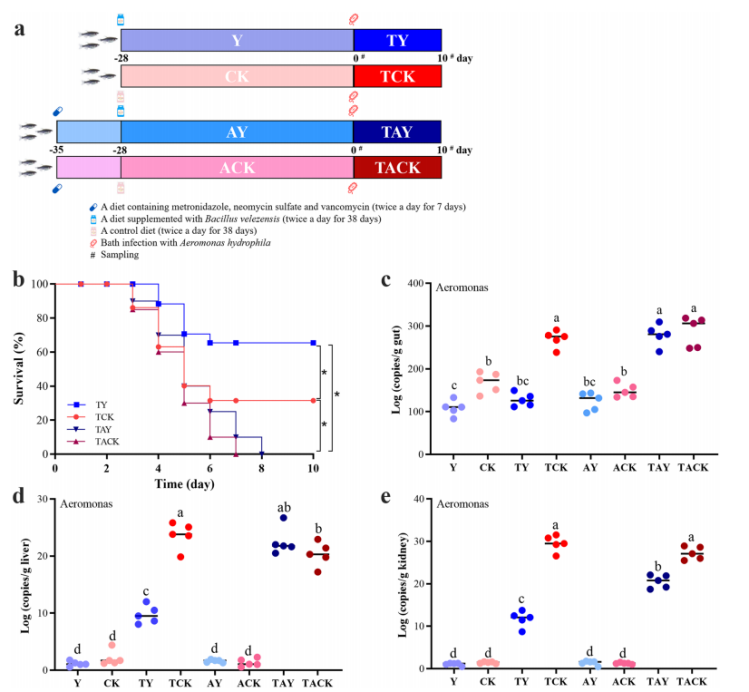

结 论
本研究结果BV1704-Y可以控制组织中的致病负荷,提高斑马鱼的存活率。基因组分析和代谢分析表明,鲸杆菌具有产生维生素B12的能力,补充维生素B12可降低肠道内的氧化还原电位,诱导肠道微生物群结构和功能的改变,改善微生物间的相互作用,增强肠道微生物群网络的稳定性。其通过影响肠道菌群网络调结肠道的紧密连接蛋白,并保护宿主免受病原体感染。这一发现可能会加深对益生菌对宿主健康影响的理解,并有助于阐明维生素B12对病原体感染的健康益处。
本研究的细菌完成图测序和分析由上海派森诺生物科技股份有限公司完成。如需进一步讨论,欢迎发邮件或者致电我们哟(邮箱地址:microsupport@personalbio.cn,联系电话:021-80118168-8617)!
文章索引: Xiaozhou Qi, Yong Zhang, Yilin Zhang, et al. Vitamin B12 produced by Cetobacterium somerae improves host resistance against pathogen infection through strengthening the interactions within gut microbiota[J]. Microbiome, (2023) 11:135.