2023-12-05

《Journal of Hazardous Materials》
影响因子
13.6
新乡医科大学在国际著名杂志《Journal of Hazardous Materials》上发表了可见光驱动 C/O-g-C3N4 通过激活过二硫酸盐有效灭活抗生素耐药菌以及抑制抗生素耐药基因转化等相关研究机制。 本研究的转录组测序以及部分分析工作由上海派森诺生物科技股份有限公司完成。
技术路线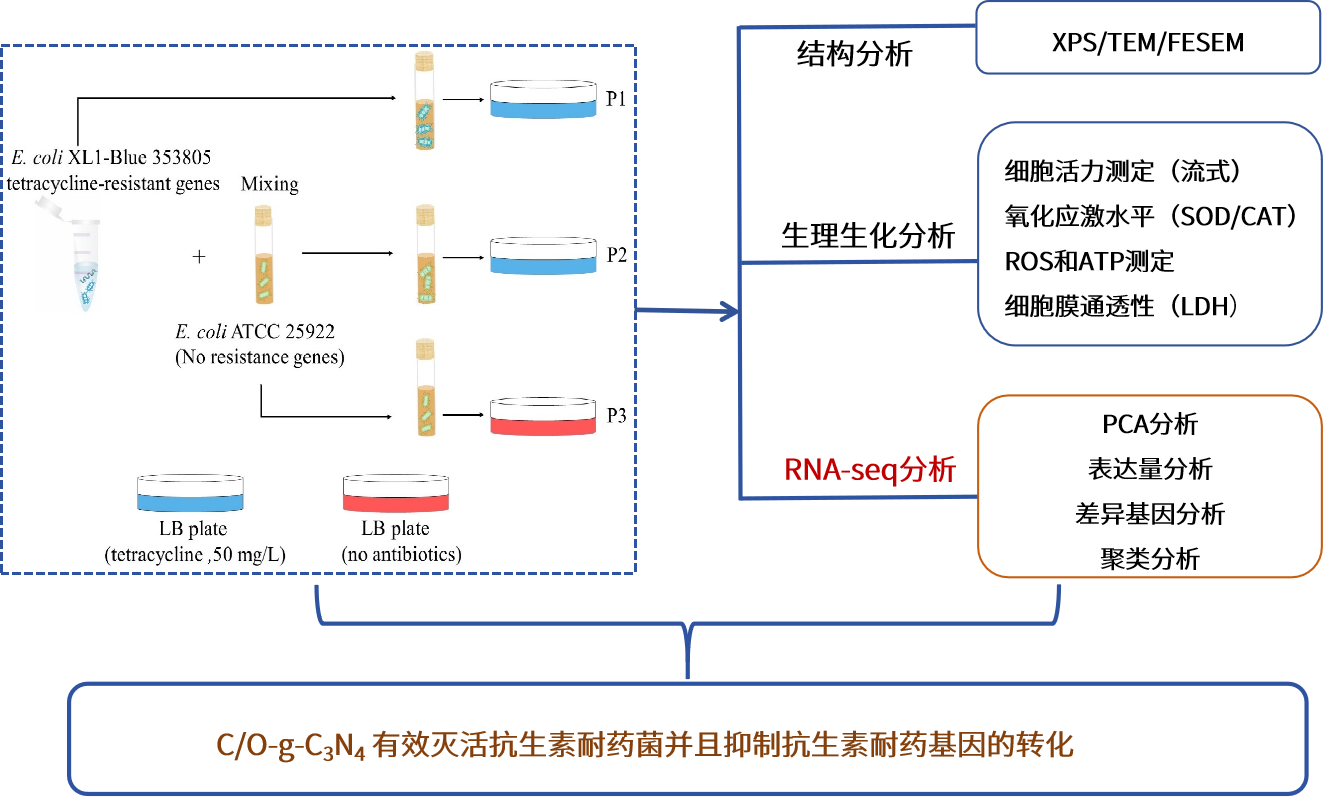
研究背景
抗生素在畜牧业、临床医学和水产品等多种领域的过度使用,严重威胁全球公共健康。近几十年来,可见光催化已成为最有前景的消毒方法之一,它能产生高活性氧化物,氮化石墨(g-C3N4)由于其成本低、无毒等优点,在光催化消毒领域得到了广泛的应用。然而,g-C3N4中光诱导载体的高度复合导致了较低的光催化效率。因此,寻找一种既能充分利用其优点又能减少其缺点的新型消毒工艺是非常有必要的。
研究材料与方法
1.实验材料 耐四环素大肠杆菌 (XL1-Blue, 353805) 、大肠杆菌 (ATCC,25922) 2.测序平台 Illumina NovaSeq 6000 3.分析方法 RNA-seq,FESEM,TEM,FCM等实验
研究结果
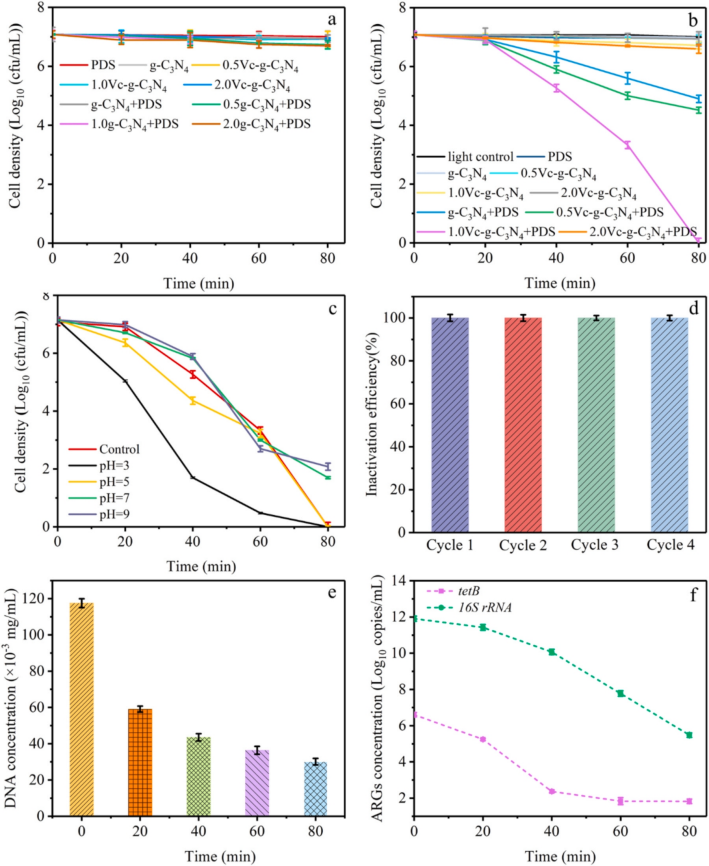
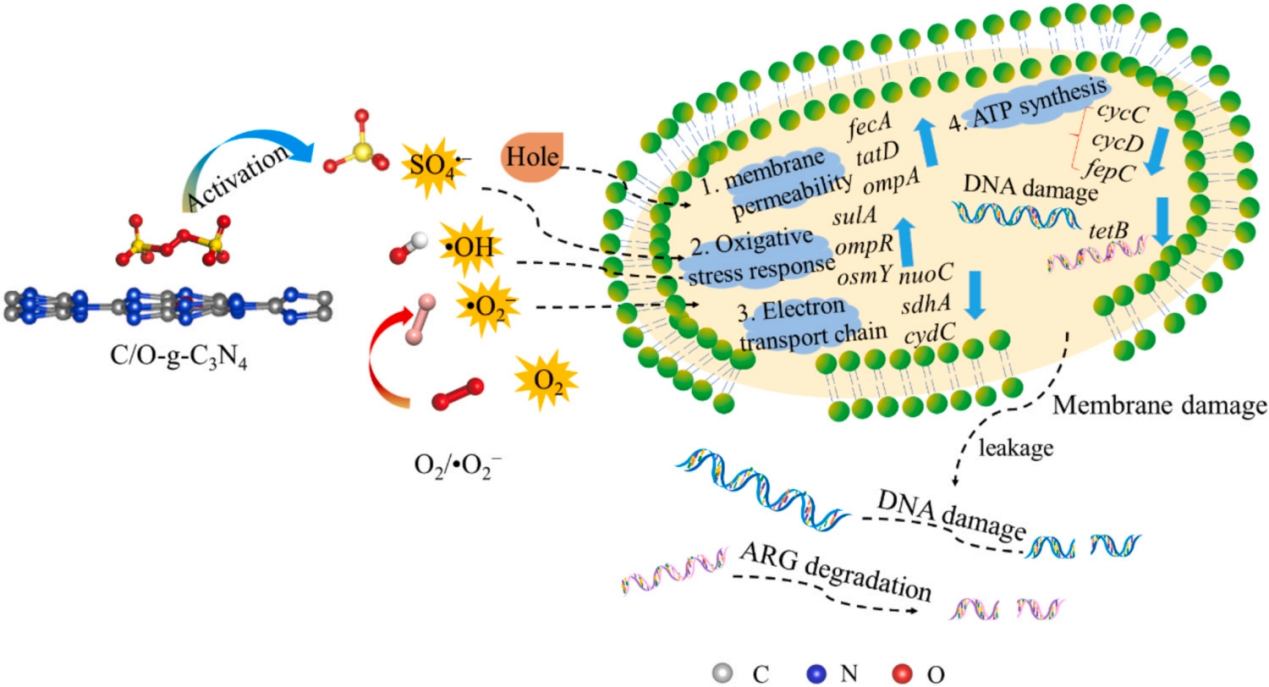
1.材料表征 利用XPS分析表明,所有样品中都存在C、N和O元素,图1a C1s 谱显示,g-C3N4在284.8、286.0和288.5 eV处有三个峰,分别表示 C-C/C=C、C-O 、 N-C=N,其中 N-C=N含量由73.75%降至46.89%,C-O含量由8.15%升至22.52%,C-C/C=C含量显著增加。在g-C3N4(图1b)的N1s谱中,随着Vc含量的增加,C/O-g-C3N4中C-N=C基团的含量减少。数据表明C-O的存在可能会改善C/O-g-C3N4和PDS体系的消毒效果。SEM结果显示如图2a所示,g-C3N4表现出厚实的体相结构,没有气孔,在1.0Vc-g-C3N4(图2b)中观察到了明显的片状结构和旺盛的气孔。TEM进一步证实了从块状g-C3N4到超薄和多孔C/O-g-C3N4的变化(图2C,d)。众所周知,多孔结构可以提供大的比表面积和丰富的孔通道,为高效消毒提供更多的反应场所和高效的物质传输通道。 图1 样本的XPS谱图 图2 SEM和TEM图像 2.ARB失活和ARGS消除 如图3a所示,PDS或光催化剂本身对细菌几乎没有影响。g-C3N4、0.5Vc-g-C3N4、 1.0Vc-g-C3N4可以在80min内分别灭活4.94、4.43和7.02log的ARB。但随着C和O含量的进一步增加,2.0Vc-g-C3N4表现出较差的失活效果。结果表明,适量的C和O显著提高了细菌的灭活,而过度则对灭菌有不利,1.0Vc-g-C3N4表现出最好的灭活效果,导致细胞膜破裂和iDNA泄漏到外部环境中。另外琼脂糖凝胶电泳显示,随着处理时间延长,靶基因条带亮度逐渐降低,说明1.0Vc-g-C3N4能有效地损伤靶基因。 图3 可见光对灭活大肠杆菌的影响 3.ARB的基因调控机制 研究者利用转录分析阐明了ARB的潜在失活机制。PCA图显示出样本良好的重复性(图4a)。利用热图展现与细胞膜、胁迫反应、细胞修复、DNA修复和细胞黏附等相关核心基因的表达水平(图4b)。与细胞膜透性相关的基因显著上调,表明处理后细胞膜透性增加。此外,1.0Vc-g-C3N4灭活体系中刺激了ROS应激反应。与胁迫反应相关的基因表达增加,表明大肠杆菌对1.0Vc-g-C3N4失活系统反应迅速。这些基因的过度表达可能是为了保护细胞免受ROS水平升高的影响。研究推测,细菌产生氧化应激来免受活性氧物种的攻击,过度的氧化应激可能会导致细菌死亡。随着灭菌时间的延长,转化频率降低。因此,较长的灭菌时间可以通过转化有效地抑制ARGs。 图4 转录组测序分析 图5 ATP含量及相关合成基因 4.机制探索 实验结果表明,1.0Vc-g-C3N4 在可见光条件下具有激活 PDS 和灭活细菌的卓越能力。与 -g-C3N4 相比,1.0Vc--g-C3N4 因其独特的结构在可见光下激活 PDS 和灭活细菌的能力更强。首先,1.0Vc-g-C3N4 中掺杂 C 和 O 引起的电子重构增强了其对可见光的吸收。其次,由于 1.0Vc--g-C3N4 和 PDS 之间的强吸附作用,光电子从 1.0Vc--g-C3N4 快速转移到 PDS。最后增加的比表面积和微孔结构,为 PDS 和大肠杆菌提供更多的活性位点。详细的消毒机制如图 9 所示。 图6 C/O-g-C3N4针对ARB和ARGS激活PDS的示意图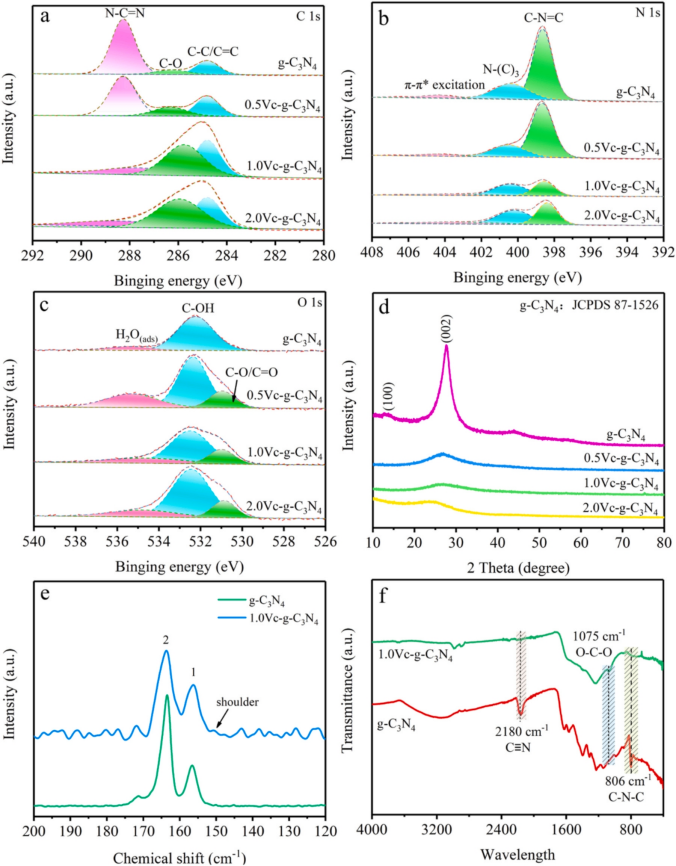



小 结
综上所述,C和O的掺杂使g-C3N4在可见光照射下表现出良好的PDS活化性能和抗菌活性。与g-C3N4相比,1.0Vc-g-C3N4对PDS的吸附和活化效率更高,从而产生更多的活性物种。这些活性物种主要引起膜通透性的变化,使它们能够进入细胞并损害细胞化合物,最终扰乱了电子传递链,阻碍了ATP的合成。此外,ARGs也被这些活性物质降解,抑制了ARGs的转化。这些发现为研究新型g-C3N4催化剂与ARGs相关的环境风险提供了理论支持。


