
2024-01-10
文章题目:Periodontitis salivary microbiota exacerbates colitis-induced anxiety-like behavior via gut microbiota
南京大学医学院附属口腔医院在《npj biofilms and microbiomes》上发表了牙周炎唾液微生物群可通过肠道微生物群加剧结肠炎诱导的焦虑样行为的研究成果。本研究中代谢组和16s检测及部分数据分析工作由上海派森诺生物科技股份有限公司完成。
研究背景 肠-脑轴是肠道与宿主脑活动之间的双向影响通道。许多宿主相关因素如口腔细菌会影响肠道功能及菌群。唾液中含有大量口腔细菌,牙周炎唾液菌群可以改变肠道菌群。然而,牙周炎唾液菌群对肠-脑轴的影响和机制仍不清楚。
技术路线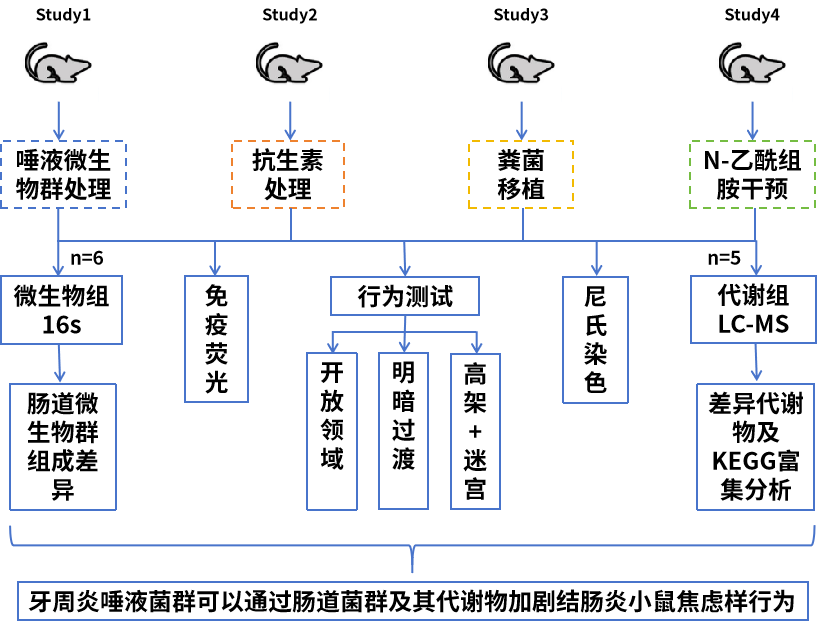
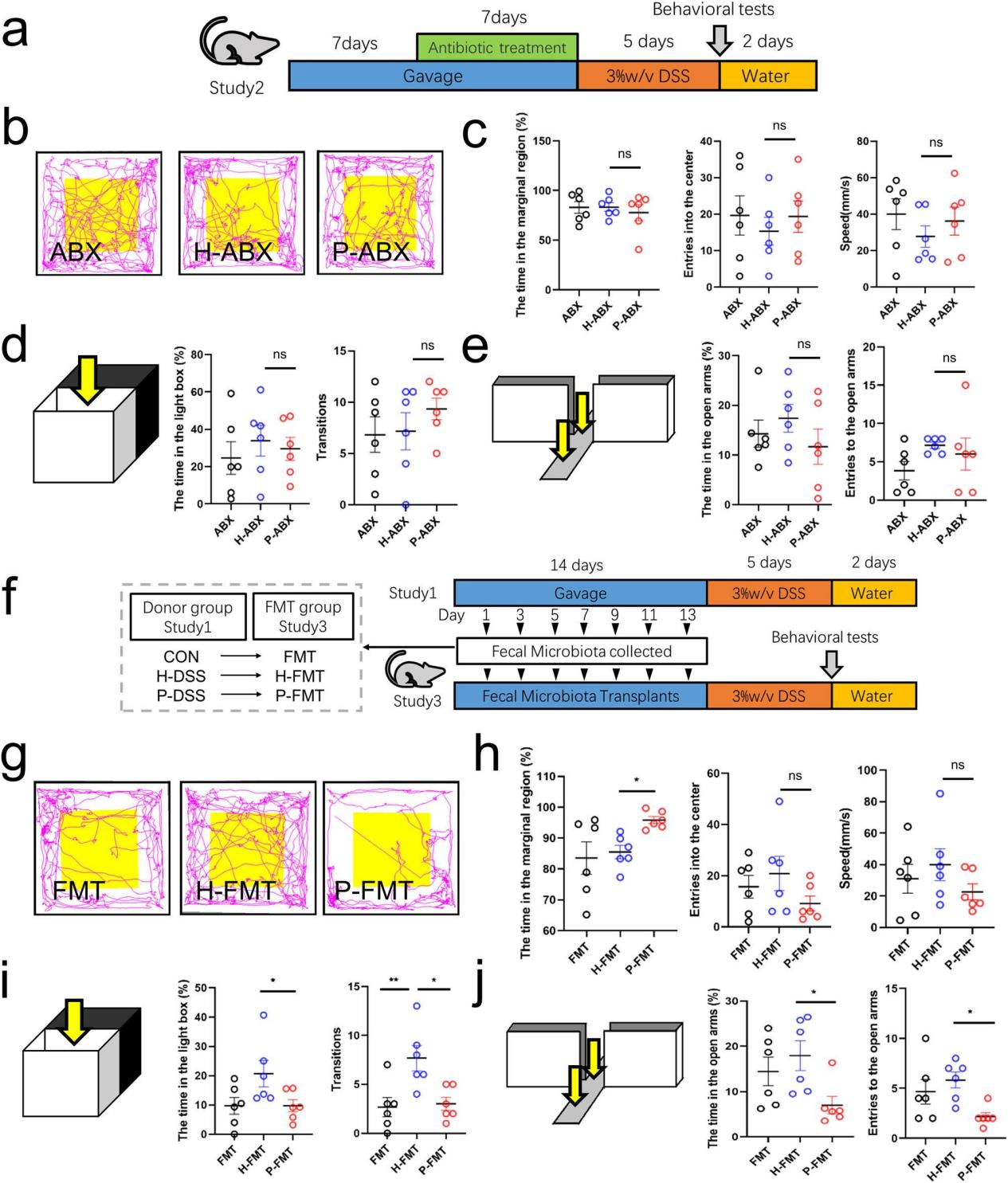
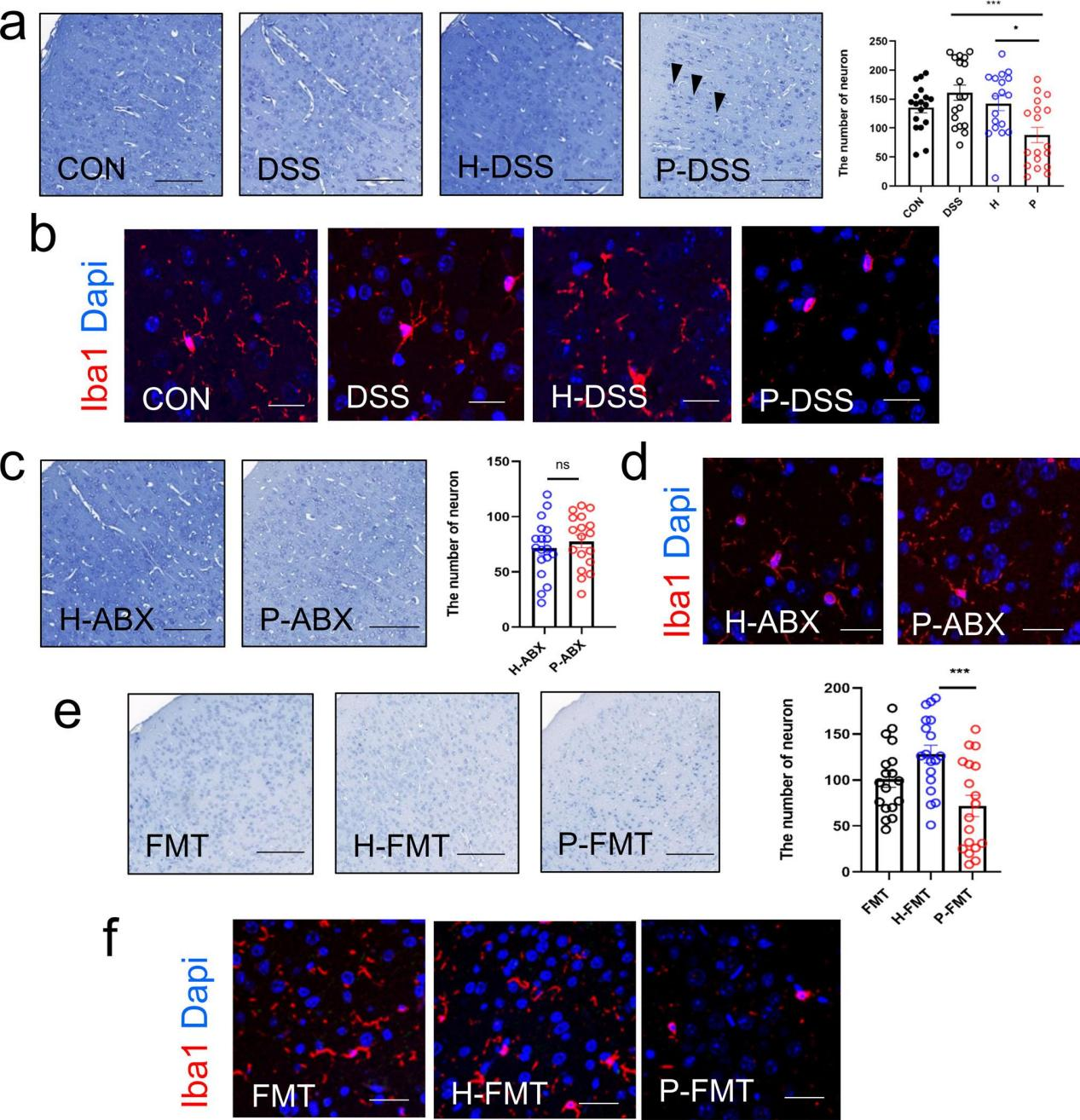
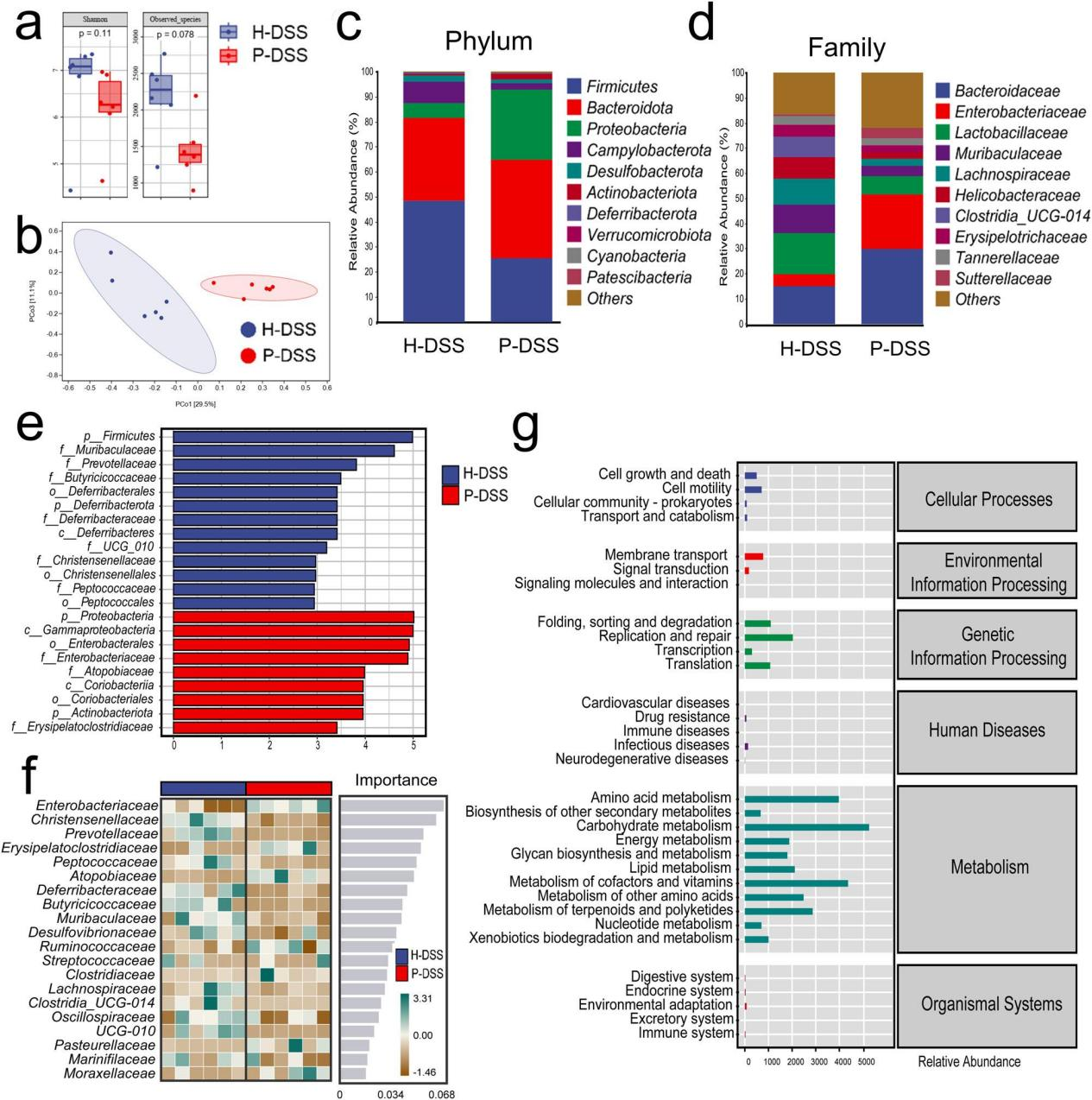
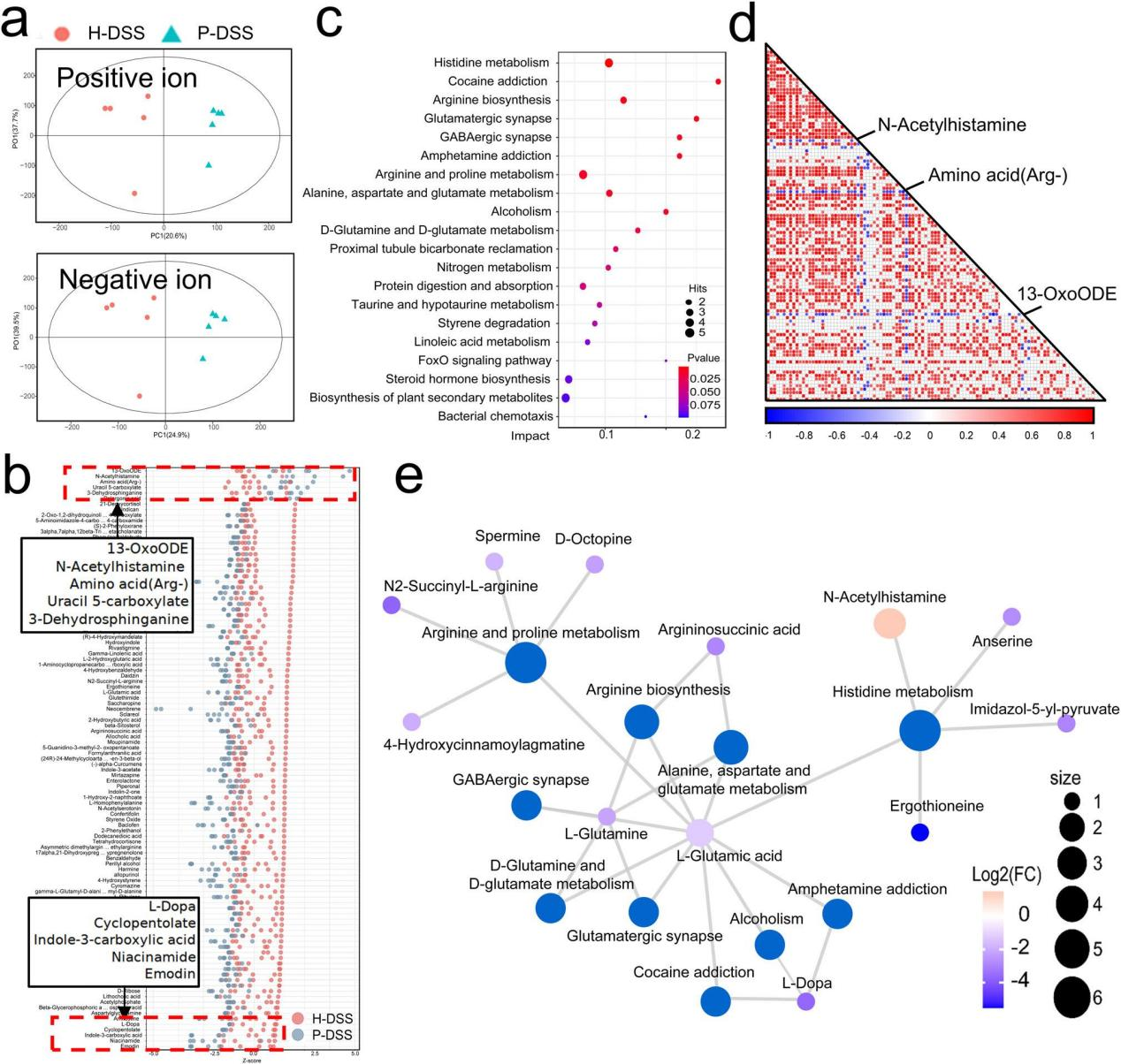
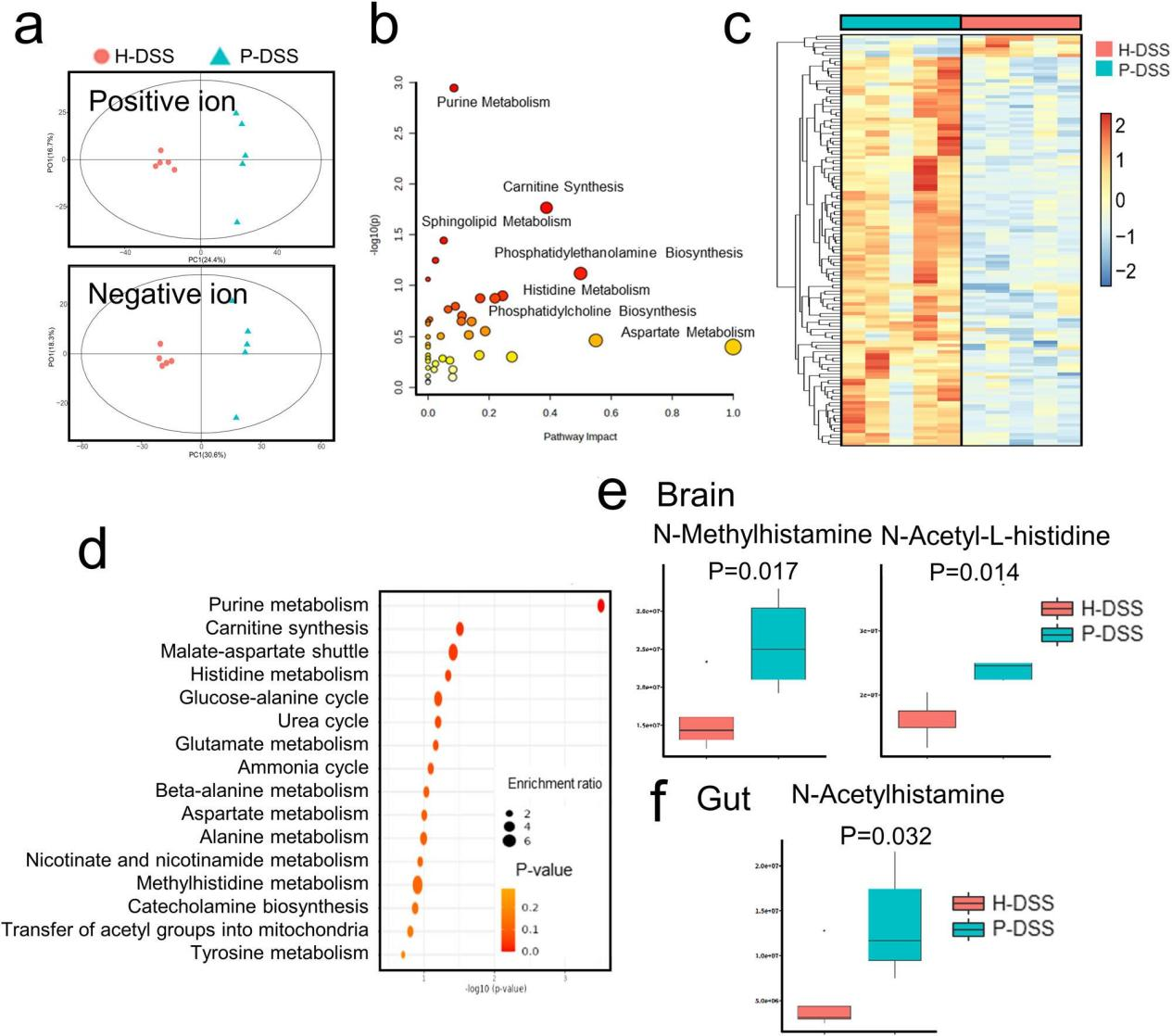
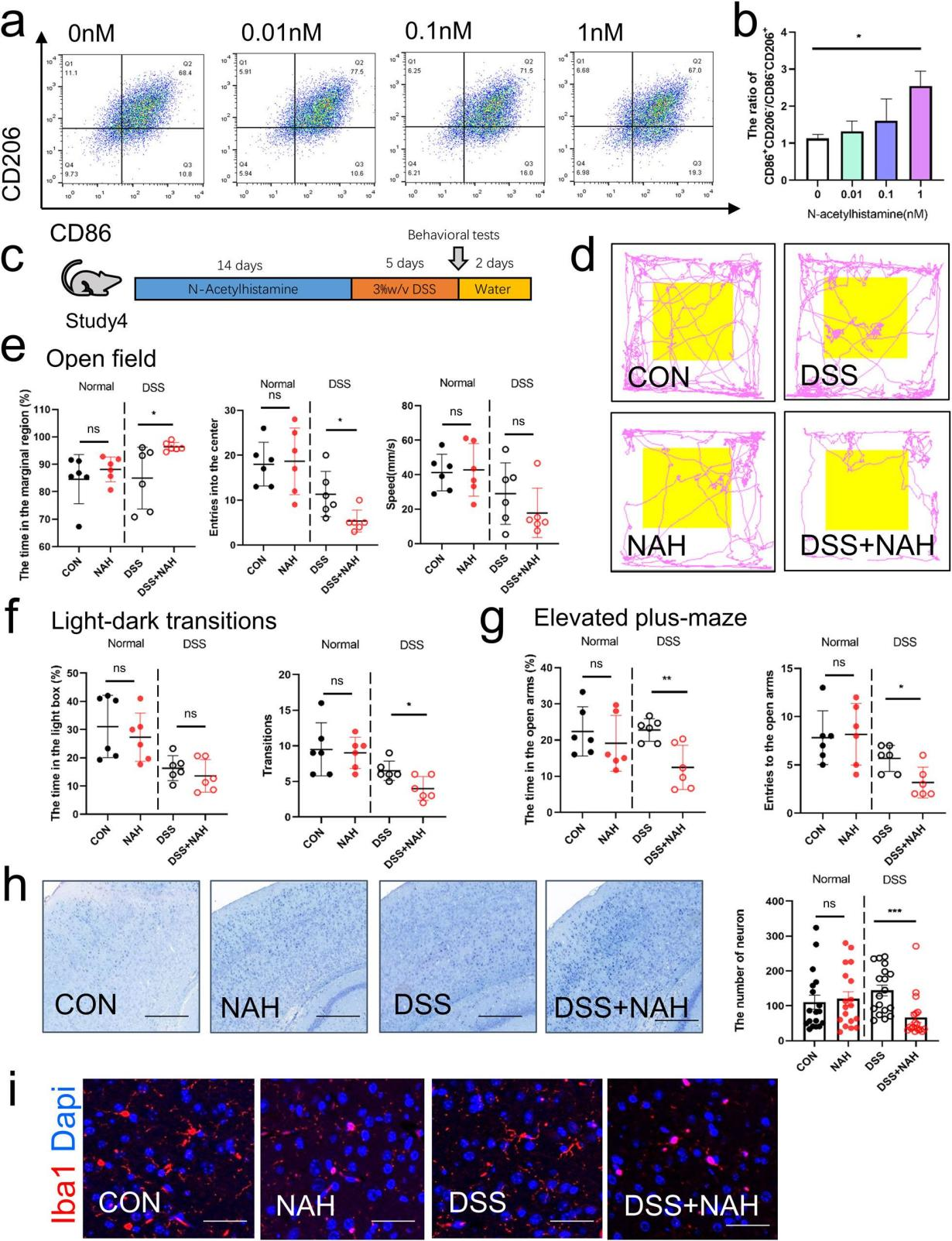
研究内容 1、牙周炎唾液微生物群加重了DSS小鼠的焦虑样行为 收集了19例患者的唾液菌群,其中牙周炎患者9例,健康者10例。基于Bray-Curtis的主坐标分析(PCoA)揭示了牙周炎唾液微生物群(PSM)和健康唾液微生物群(HSM)之间的差异(图1a)。PSM的α-多样性明显高于HSM(图1b)。在门水平上,与HSM相比,PSM中厚壁菌门的相对丰度降低了(图1c)。在科水平上,与HSM相比,PSM中Streptococcaceae的相对丰度降低,Porphyromonadaceae的相对丰度增加(图1d)。根据线性判别分析效应大小(LEfSe)分析,Porphyromonadaceae和Spirochaetaceae是PSM中主要的代表性科级分类群,而Streptococcaceae是HSM在科级水平上的代表性分类群(图1e)。作者将混合的唾液微生物群灌胃给24只小鼠,使用DSS成功诱导结肠炎(图1f)。 为了观察唾液微生物群对焦虑样行为的影响,我们进行了开放性、明暗转换和高架+迷宫的行为测试。在空旷区,DSS组在边缘区停留的时间较多,在中心区停留的时间较少,且速度较CON组慢。与H-DSS组相比,P-DSS组在边缘区域停留的时间更长,速度更低(图1g-h)。在明暗转换中,DSS组的转换频率显著低于CON组。与H-DSS组相比,P-DSS组在灯箱中花费的时间和在明暗箱之间转换的频率显著降低(图1i)。在高架+迷宫实验中,DSS组小鼠的张开臂活动时间和进入张开臂的次数均低于CON组,P-DSS组小鼠的张开臂活动时间也低于H-DSS组(图1j)。上述结果表明,DSS加重了焦虑行为,而PSM加重了DSS诱导的类焦虑行为。 图1 牙周炎唾液微生物群加剧葡聚糖硫酸钠(DSS)小鼠的焦虑样行为 2、肠道菌群介导PSM加重DSS诱导的焦虑样行为的作用 为了研究唾液微生物群改变的肠道微生物群对焦虑样行为的影响,作者在牙周炎唾液微生物群灌胃后给DSS小鼠抗生素治疗1周(图2a)。ABX组、H-ABX组和P-ABX组在边缘区域的活动时间和速度以及在空旷区域进入中心区域的次数上均无显著差异(图2a-c)。抗生素治疗后各组之间的明暗转换和高架迷宫行为结果也无显著差异(图2d-e)。这些结果表明,抗生素治疗消除了两组之间的行为差异,表明肠道微生物群是PSM加剧焦虑样行为的关键因素。 为了进一步验证肠道菌群在焦虑样行为中的作用,我们从唾液菌群灌胃的小鼠中移植新鲜粪便菌群,并进行DSS治疗,观察行为变化(图2f)。P-FMT组DSS小鼠在空地边缘区域停留的时间明显长于H-FMT组。它们在边缘区域的速度和进入空地中心区域的频率也有所降低,但不明显(图2g-h)。与H-FMT组相比,P-FMT组在光照下花费的时间、明暗盒子之间转换的频率、张开手臂的活动时间和进入张开手臂的次数显著减少(图2i-j)。这些行为结果表明,P-FMT组表现出与PSM相似的加剧焦虑样行为,证实PSM通过肠道微生物群加剧了DSS诱导的焦虑样行为。 图2 肠道微生物群是牙周炎的关键,唾液微生物群加剧葡聚糖硫酸钠诱导的焦虑样行为 3、PSM通过肠道微生物群损伤神经元并激活大脑皮层的小胶质细胞 接下来,我们探讨了PSM过程中焦虑相关的病理改变对焦虑样行为的影响,包括免疫荧光法观察小胶质细胞形态和尼氏染色法观察正常神经元数量。Nissl染色结果显示,与H-DSS组相比,P-DSS组大鼠大脑皮层正常神经元数量明显减少,胞质实变,形状不规则,神经元染色加深(黑色箭头;图3 a)。小胶质细胞的生物标志物电离钙结合适配器分子1(Iba1)的染色显示,与大脑皮层的H-DSS组相比,P-DSS组的小胶质细胞明显皱缩,表明小胶质细胞被激活(图3b)。 为了确定肠道微生物群在大脑病理改变中的作用,我们还检测了抗生素处理和粪便微生物群移植小鼠中的小胶质细胞和神经元。在抗生素治疗小鼠中,H-ABX组和P-ABX组之间神经元数量和小胶质细胞活化的所有差异都消失了(图3c-d)。粪便微生物群移植实验结果显示,P-FMT组与H-FMT组相比,大脑皮层神经元数量和小胶质细胞激活明显减少(图3e-f)。因此,PSM可以减少正常神经元的数量,并通过肠道微生物群激活小胶质细胞,从而加剧焦虑样行为。 图3 牙周炎唾液微生物群通过肠道微生物群减少神经元数量并激活大脑皮层小胶质细胞 4、PSM改变了DSS小鼠肠道菌群的组成 为了研究肠道微生物群的变化,作者使用16s基因测序检测了H-DSS组和P-DSS组的肠道微生物群组成。与H-DSS组相比,P-DSS组α-多样性降低(图4a)。PCoA显示两组之间肠道菌群组成存在显著差异(图4b)。在门水平上,P-DSS组厚壁菌门的相对丰度低于H-DSS组(图4c)。在科水平上,P-DSS组Enterobacteriaceae和Bacteroidaceae的相对丰度高于H-DSS组(图4d)。LEfSe分析表明,P-DSS组的代表性微生物群属于Enterobacteriaceae,而H-DSS组主要是Firmicutes phylum、Muribaculacae和Prevotellaceae(图4e)。随机森林分析结果预测Enterobacteriaceae和Christensenellaceae可能是在P-DSS组中发挥作用的重要细菌群(图4f)。最后,基于PICRUSt2标记的基因序列对H-DSS和P-DSS组肠道微生物群的功能预测表明,这些细菌的主要功能途径富含代谢相关任务,包括氨基酸代谢、碳水化合物代谢、辅助因子和维生素的代谢(图4g)。这些结果表明,PSM导致肠道菌群紊乱,这些紊乱可能与代谢物极化为氨基酸和碳水化合物代谢的改变有关。 图4 牙周炎唾液菌群改变肠道菌群组成 5、PSM引起DSS小鼠肠道代谢物的改变 我们使用液相色谱-质谱法研究肠道代谢物的变化。分别对正负离子模式下筛选的代谢物进行正交偏最小二乘判别(OPLS-DA)分析,发现P-DSS组和H-DSS组肠道代谢物存在显著差异(图5a)。采用Z-score分析观察这些代谢物的相对水平;分别筛选出了P-DSS组和H-DSS组中最丰富的前五种代谢物(图5b)。差异代谢物富集分析显示,氨基酸代谢(组氨酸代谢和精氨酸生物合成)和神经递质相关途径(可卡因成瘾、谷氨酸能突触和氨基丁酸能突触)是主要途径,其中组氨酸代谢显著变化(图5c)。通过Spearman相关分析确定代谢物之间的相关性,与其他代谢物相比,NAH和氨基酸(arg-)具有明显相反的趋势,提示这些代谢物可能起着关键作用(图5d)。最后,构建了这些代谢物及其途径的网络分析,氨基酸代谢(如组氨酸、精氨酸和脯氨酸)构成了大多数代谢物参与的途径,其中l -谷氨酸和l -谷氨酰胺是关键节点,而在P-DSS组中,NAH是唯一参与这些途径的高表达代谢物(图5e)。值得注意的是,一些肠道代谢产物和相关途径,如GABA能突触和左旋多巴(在H-DSS组中含量较高),是参与焦虑样行为的神经递质。值得注意的是,一些肠道代谢产物和相关途径,如GABA能突触和左旋多巴(在H-DSS组中含量较高),是参与焦虑样行为的神经递质。 图5 牙周炎灌胃后肠道代谢物的改变 6、PSM引起DSS处理小鼠脑代谢异常 接下来,我们检查了大脑代谢,以探索影响焦虑样行为的关键代谢产物。正离子模式和负离子模式的OPLS-DA分析结果显示,H-DSS组和P-DSS组之间的代谢物存在显著差异(图6a)。对这些代谢物进行富集分析发现,它们主要富集于磷脂酰乙醇胺生物合成、组氨酸代谢、嘌呤代谢、肉碱合成、鞘脂代谢和天冬氨酸代谢(图6b)。此外,与神经元相关的磷脂酰乙醇胺生物合成、磷脂酰胆碱生物合成和鞘脂代谢等通路也得到了丰富。代谢物表达差异如图6c所示。P-DSS组主要差异代谢物高表达;因此,我们对P-DSS组升高的代谢物进行富集分析,发现嘌呤代谢、肉毒碱合成、苹果酸-天冬氨酸穿梭、组氨酸代谢和葡萄糖-丙氨酸循环是前五大富集途径(图6d)。N-乙酰-L-组氨酸和N-甲基组胺在P-DSS组的脑代谢中高表达(图6e),而NAH在P-DSS组的肠道代谢中高表达(图6f)。为了进一步探讨肠道微生物群与代谢物之间的关系,我们基于脑代谢物、肠道代谢物和肠道微生物群的Spearman相关分析建立了相关网络(P < 0.05)。以上结果表明,肠道微生物群与大脑和肠道代谢有关,组胺相关代谢物是PSM对焦虑样行为影响的关键介质。 图6 牙周炎唾液微生物群导致脑代谢的改变 7、N-乙酰组胺可能是PSM通过肠-脑轴促进焦虑的中介 最后,为了验证肠道代谢物的作用,我们首先使用P-DSS组肠道中高表达的组胺相关物质NAH刺激小胶质细胞。我们发现,NAH可以增加小鼠BV-2小胶质细胞中CD86+/CD206 -的表达,而添加NAH后CD206+/CD86 -的表达下降,特别是在1 nM时(图7a, b)。然后我们给DSS和非DSS小鼠灌胃10 nM的NAH(图7c)。在行为水平上,NAH显著增加了DSS处理小鼠在边缘区域停留的时间,降低了进入空地中心区的频率(图7d-e)。同样,与DSS组相比,DSS + NAH组的过渡时间和进入张开臂的时间更短,进入张开臂的频率更低(图7f-g)。在组织学水平上,Nissl染色显示NAH灌胃使DSS小鼠正常神经元数量减少(图7h)。免疫荧光显示NAH激活的小胶质细胞,在DSS + NAH组中最为明显(图7i)。这些发现表明,肠道代谢物,如NAH,是促进DSS小鼠PSM焦虑样行为的关键物质。 图7 N-乙酰组胺可能是PSM通过肠-脑轴促进焦虑的中介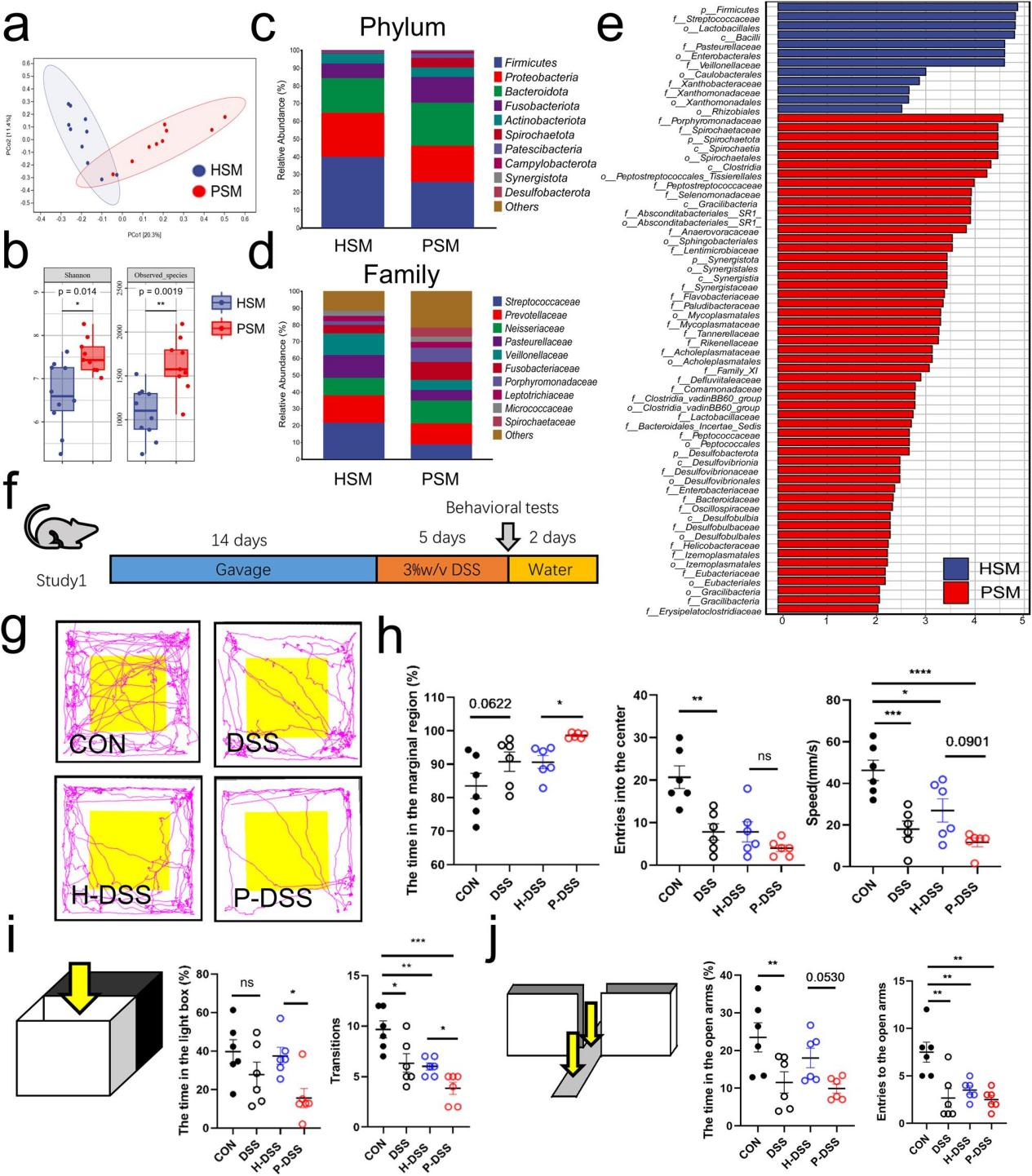
研究结论 研究将健康人唾液菌群及牙周炎患者唾液菌群灌胃至DSS诱导的小鼠,发现牙周炎唾液菌群可以加剧小鼠的焦虑样行为。抗生素处理及粪菌移植实验验证了肠道菌群是牙周炎唾液菌群促进焦虑样行为的关键因素。最后,通过代谢组学分析筛选出关键代谢物,并验证其在牙周炎影响大脑活动中的关键作用。该研究发现牙周炎唾液菌群可以通过肠道菌群及其代谢物加剧结肠炎小鼠焦虑样行为,表明牙周疾病可通过肠-脑轴影响脑活动,提示防治牙周疾病的重要性。
原文索引: Qian J, Lu J, Cheng S, Zou X, Tao Q, Wang M, Wang N, Zheng L, Liao W, Li Y, Yan F. Periodontitis salivary microbiota exacerbates colitis-induced anxiety-like behavior via gut microbiota. NPJ Biofilms Microbiomes. 2023 Dec 7;9(1):93. doi: 10.1038/s41522-023-00462-9. PMID: 38062089; PMCID: PMC10703887.