期刊:《The ISME Journal》
影响因子:9.18
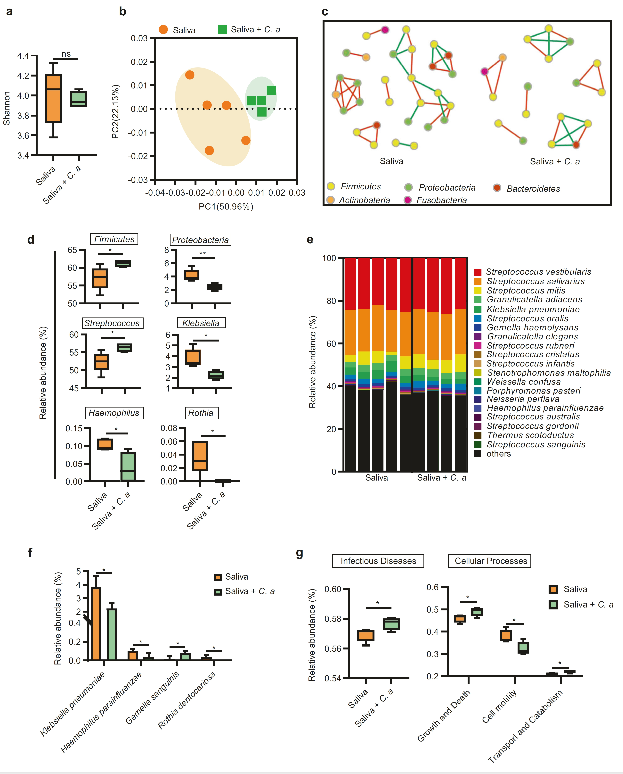
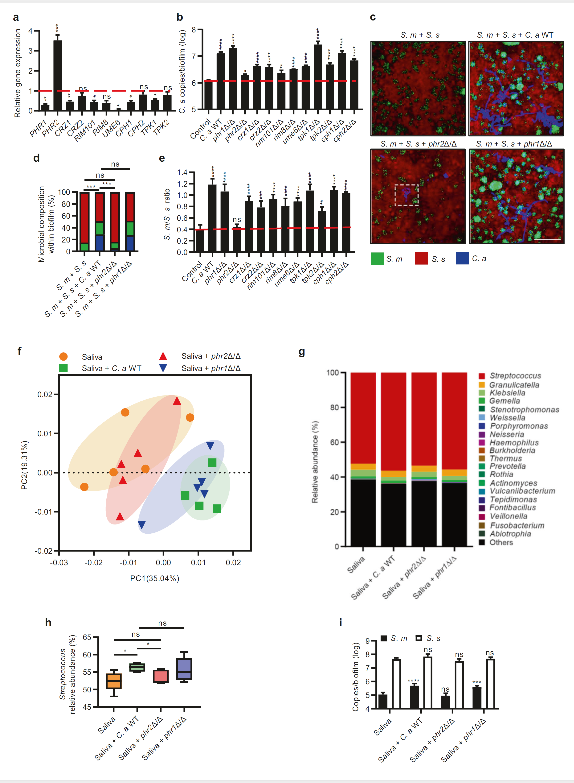
近日,派森诺与四川大学华西口腔医学院合作,在微生态领域期刊《The ISME Journal》(影响因子:9.18)上发表科研成果,可喜可贺!本研究利用PacBio三代测序技术,通过16S rRNA基因全长测序,发现在体外龋齿模型及大鼠龋齿模型中,白色念珠菌的定植可改变口腔微生物菌群的组成,增加口腔生物膜的致龋齿能力,从而恶化龋齿的病变程度,揭示了该菌种对根面龋的微生物生态学作用及致病机制。 研究背景 根面龋是一种常见的微生物感染性口腔疾病,老年人根龋的患病率达相对较高,是根面龋的高发人群,也是口腔白色念珠菌感染的易感人群。根面龋的发生与存在于微生物生物膜中的产酸物种(如变形链球菌)的富集和产酸较少的共生体(如血链球菌)有关,因此微生物失衡在龋齿发生过程中起着关键作用。 白色念珠菌是一种共生真菌,健康个体口腔携带白色念珠菌量培养率为18.5-40.9%,携带率通常在免疫力低下的个体中较高。白色念珠菌能与其他口腔微生物形成紧密的互作关系,对微生物生物膜的毒力产生显著影响。与健康人群口腔中的白色念珠菌相比,定植于根龋病变的白色念珠菌的代谢活性、糖转运、胁迫耐受性和pH调节等相关基因表达上调,进一步突显了白色念珠菌在根龋病变发生发展过程中的潜在作用。然而,白色念珠菌对根龋的微生物生态学和致病机制,以及与其他微生物跨界相互作用的关键因素尚不清楚。 研究方法 测序区域:16S rRNA基因近全长 测序平台:PacBio Sequel三代测序 样本数量:为了探讨白色念珠菌、PHR1基因和PHR2基因与口腔唾液生物膜微生物组成之间的关系,实验人员收集无白色念珠菌感染的健康者(经PCR验证)的唾液,建立唾液源生物膜,并分成以下四个处理组: ● 对照组:无白色念珠菌感染的唾液源生物膜样本5例 ● 处理组1:白色念珠菌感染的唾液源生物膜样本4例 ● 处理组2:缺失PHR2基因的白色念珠菌感染的唾液源生物膜样本5例 ● 处理组3:缺失PHR1基因的白色念珠菌感染的唾液源生物膜样本5例 研究结果 1. 白色念珠菌的定植改变口腔唾液微生物生物膜的平衡 白色念珠菌的定植导致口腔微生物生物膜的Shannon指数降低,微生物群落的多样性降低,同时破环了生物膜中微生物之间的相互作用网络,降低了微生物间的协同效应。通过在门水平和种水平上物种相对丰度以及预测代谢通路变化的比较,发现白色念珠菌的感染导致多种微生物的相对丰度和代谢通路存在差异性(图1)。 图1 白色念珠菌的定植改变口腔唾液微生物生物膜的平衡 2. PHR2基因有助于致龋条件下,增加白色念珠菌在口腔唾液微生物生物膜上定植的可能性 PCoA分析发现,在有无白色念珠菌或其PHR1/PHR2缺失突变体的情况下,对照组和处理组2的微生物组成更加相似,而处理组1和处理组3的微生物组成更加相似,同时链球菌属的相对丰度表现出同样的趋势。进一步采用体外人工龋模型和根龋大鼠模型实验同样证实,PHR2基因是在致龋条件下,白色念珠菌成功在微生物生物膜定植的主要因素。 图2 PHR2基因有助于白色念珠菌在致龋条件下,在微生物生物膜定植 研究结论 ● 相比于龋齿患者及健康人的健康牙根表面,龋齿患者的根龋病变处的白色念珠菌定植率显著升高(71.4% vs. 31.4% vs. 28.6%); ● 白色念珠菌定植通过改变口腔生物膜的微生物生态,增加了其龋齿的致龋性,形成了酸性增强的多菌生物膜,加重了牙齿脱矿和龋损的严重程度; ● 在体外及大鼠龋齿模型中,白色念珠菌的定植可与链球菌属互作,并改变口腔生物膜中的菌群组成,增加口腔生物膜的产酸能力及致龋齿性,从而恶化龋齿病变严重程度及牙齿矿物质流失; ● 白色念珠菌PHR2基因参与调控白色念珠菌在致龋微环境中的定植、生长与毒力,在致龋条件下,PHR2基因是白色念珠菌成功在微生物生物膜定植的主要因素。 总 结 本研究利用PacBio三代测序技术,通过16S rRNA基因全长测序,对口腔微生物组种水平的变化进行了“高分辨率”的精细研究,揭示了白色念珠菌在促根面龋发生发展过程中的作用,及其在致龋微环境下定植并调控牙菌斑微生态的关键因子,有望成为根面龋生态防治的潜在靶点,为根面龋的防治提供了新的思路。